题目内容
(16分)含苯酚的工业废水处理的流程图如下所示:
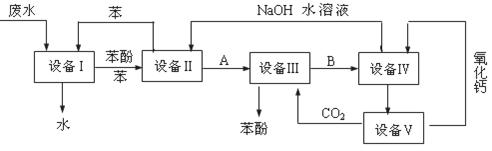
(1)上述流程里,设备Ⅰ中进行的是 操作(填操作名称),实验室里这一步操作可以用 进行(填仪器名称)。
(2)由设备Ⅱ进入设备Ⅲ的物质A是 ,由设备Ⅲ进入设备Ⅳ的物质B是
(3)在设备Ⅲ中发生反应的化学方程式为
(4)在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和 ,通过
操作(填操作名称)可使产物相互分离。
(5)图中,能循环使用的物质是C6H6、CaO、

(1)上述流程里,设备Ⅰ中进行的是 操作(填操作名称),实验室里这一步操作可以用 进行(填仪器名称)。
(2)由设备Ⅱ进入设备Ⅲ的物质A是 ,由设备Ⅲ进入设备Ⅳ的物质B是
(3)在设备Ⅲ中发生反应的化学方程式为
(4)在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和 ,通过
操作(填操作名称)可使产物相互分离。
(5)图中,能循环使用的物质是C6H6、CaO、
(1)萃取、分液 分液漏斗 (2)C6H5ONa NaHCO3
(3)C6H5ONa+CO2+H2O→C6H5OH+NaHCO3 (4)CaCO3 过滤 (5)NaOH溶液 CO2
(3)C6H5ONa+CO2+H2O→C6H5OH+NaHCO3 (4)CaCO3 过滤 (5)NaOH溶液 CO2
试题分析:(1)从工业废水与苯进入设备Ⅰ得到苯酚、苯的溶液与无酚工业废水(此废水可以排放),说明在设备Ⅰ中进行的是萃取,利用苯与苯酚具有相似的结构,将苯酚从工业废水里抽提出来,用分液的方法将下层的工业废水放出排放,上层的苯酚苯溶液进入设备Ⅱ。
(2)盛有苯酚苯溶液的设备Ⅱ中注入氢氧化钠溶液,此时,具有酸性的苯酚跟氢氧化钠发生中和反应,生成苯酚钠和水。苯酚钠是离子化合物,易溶于水中。伴随上述化学反应的发生,在设备Ⅱ中的液体分为两层,上层是苯层,下层是苯酚钠的水溶液(即设问中的物质A)。上层的苯通过管道送回设备Ⅰ中继续萃取工业废水中的苯酚,循环使用,下层的苯酚钠(A)溶液进入设备(Ⅲ)。
(3)在盛有苯酚钠溶液的设备Ⅲ中,通入过量的二氧化碳气,这两种物质间发生化学反应,生成苯酚和碳酸氢钠,这个化学实质是较强酸制取较弱的酸,化学方程式为C6H5ONa+CO2+H2O→C6H5OH+NaHCO3。
在析出的苯酚中含有微量水,呈油状液体,沉于设备Ⅲ液体的下层,经分液后再精馏可得苯酚。上层液体B是溶液,经管道输送进入设备Ⅳ。
(4)盛有碳酸氢钠溶液的设备Ⅳ中,加入生石灰,生石灰与碳酸氢钠溶液里的水化合变为熟石灰,随后发生复分解反应,生成和白色沉淀碳酸钙沉淀,溶液与沉淀通过过滤分离,即得到碳酸钙固体。
反应所得溶液,通过管道进入设备Ⅱ,循环使用;所得沉淀进入设备Ⅴ。
(5)在设备Ⅴ中的原料是固体,所得的产品是氧化钙和二氧化碳,由此可知,设备Ⅴ实质应是石灰窑,即碳酸钙在高温下分解生成氧化钙和CO2,反应所得二氧化碳通入设备Ⅲ,反应所得氧化钙进入设备Ⅳ。
综上所述,在含苯酚工业废水提取苯酚的工艺流程中,苯、氧化钙、氢氧化钠、二氧化碳4种物质均可以循环使用,理论上应当没有消耗。
点评:该题是高考中的常见考点,试题综合性强,难度较大,对学生的思维能力提出了更高的要求,学生不易得分。该题在注重基础性知识考查的同时,侧重能力的训练和解题方法的指导,有利于培养学生的逻辑推理能力,和发散思维能力,提高学生分析问题、解决问题的能力。

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目