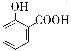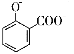题目内容
【题目】下列说法错误的是( )
A. 某些花岗石产生氡(22288Rn),该元素的相对原子质量为222
B. Se是人体必需的微量元素, 7834Se和8034Se互为同位素
C. F2通入氯化钠溶液中,生成的主要气体为O2
D. 136CNMR(核磁共振)可用于含碳化合物的结构分析,![]() C的中子数为7
C的中子数为7
【答案】A
【解析】
A. 质量数指的是质子数与中子数的和,而不同核素的质量数不同,即一个元素可以有多个质量数,相对原子质量为各核素的平均相对质量所以同种元素的相对原子质量只有一个数值,故A错误;
B. ![]() 和
和![]() 的质子数均为34,中子数分别为44、46,则二者互为同位素,故B正确;
的质子数均为34,中子数分别为44、46,则二者互为同位素,故B正确;
C. F2通入氯化钠溶液中,F2与水反应生成氟化氢和氧气,反应方程式为:2F2+2H2O=4HF +O2,故C正确;
D. ![]() C中质子数为6,质量数为13,中子数=质量数-质子数=13-6=7,故D正确。
C中质子数为6,质量数为13,中子数=质量数-质子数=13-6=7,故D正确。
故选A。

 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
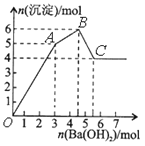
同步奥数系列答案【题目】向FeCl3、Al2(SO4)3的混和溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如下图所示。沉淀的生成的pH列于下表(已知:偏铝酸钡易溶于水)。以下推断正确的是
氢氧化物 | 溶液pH | |
开始沉淀 | 沉淀完全 | |
Fe(OH)3 | 2.3 | 3.4 |
Al(OH)3 | 3.3 | 5.2 |
A. OA段产生的沉淀为BaSO4和Fe(OH)3
B. 据图计算原溶液中c(Cl-)=c(SO42-)
C. AB段可能发生的反应是:2SO42-+ 2Ba2++ Al3++3OH-=2BaSO4↓+Al(OH)3↓
D. C点溶液呈碱性是因为AlO2-水解,离子方程式为:AlO2-+2H2O=Al(OH)3+OH-
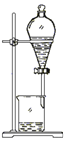
【题目】下述实验方案能达到实验目的的是( )
编号 | A | B | C | D |
实验方案 |
|
|
|
|
实验目的 | 实验室制备乙酸乙酯 | 分离乙酸和水 | 验证溴乙烷在氢氧化钠乙醇溶液中发生消去反应产生的乙烯 | 收集乙烯并验证它与溴水发生加成反应 |
A. A B. B C. C D. D