题目内容
【题目】下表是元素周期表短周期的一部分

(1)①~⑦元素中金属性最强的元素在元素周期表中的位置是___________。
(2)表中元素⑥的原子结构示意图为___________。
(3)④与⑤形成的化合物的化学键类型为_______,该化合物的电子式为____________。
(4)表中元素②、③、⑦最高价含氧酸的酸性由强到弱的顺序是___________(填化学式,下同);④所在主族的前四种元素的单质分别与氢气化合形成的气态氢化物的稳定性由强到弱的顺序是_________。
(5)表中元素②的单质与③的最高价含氧酸反应的化学方程式为___________________。
【答案】 第三周期第ⅡA族 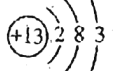 离子键
离子键 ![]() HNO3>H2CO3 >H2SiO3 HF>HCl>HBr>HI C+4HNO3(浓)
HNO3>H2CO3 >H2SiO3 HF>HCl>HBr>HI C+4HNO3(浓) ![]() CO2↑+4NO↑+2H2O
CO2↑+4NO↑+2H2O
【解析】根据元素周期表,①为H元素;②为C元素;③为N元素;④为F元素;⑤为Mg元素;⑥为Al元素;⑦为Si元素;⑧为S元素。
(1)①~⑦元素中金属性最强的元素为镁,在元素周期表中位于第三周期第ⅡA族,故答案为:第三周期第ⅡA族;
(2)表中元素⑥为铝,原子结构示意图为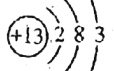 ,故答案为:
,故答案为: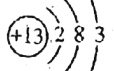 ;
;
(3) ④为F元素;⑤为Mg元素,氟化镁属于离子化合物,含有离子键,电子式为![]() ,故答案为:离子键;
,故答案为:离子键;![]() ;
;
(4)元素的非金属性越强,最高价含氧酸的酸性越强,表中元素②、③、⑦最高价含氧酸的酸性由强到弱的顺序为HNO3>H2CO3 >H2SiO3;④为F元素,元素的非金属性越强,气态氢化物越稳定,则卤素的气态氢化物的稳定性由强到弱的顺序为HF>HCl>HBr>HI,故答案为:HNO3>H2CO3 >H2SiO3;HF>HCl>HBr>HI ;
(5)碳与浓硝酸反应生成二氧化碳、二氧化氮和水,反应的化学方程式为C+4HNO3(浓) ![]() CO2↑+4NO↑+2H2O,故答案为:C+4HNO3(浓)
CO2↑+4NO↑+2H2O,故答案为:C+4HNO3(浓) ![]() CO2↑+4NO↑+2H2O。
CO2↑+4NO↑+2H2O。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案【题目】为提纯下列物质(括号内为杂质),选用的试剂和分离方法不正确的是
物质 | 试剂 | 分离方法 | |
A | 淀粉溶液(NaCl) | 水 | 渗析 |
B | CaCO3(CaO) | 水 | 过滤 |
C | KCl溶液(I2) | 酒精 | 萃取 |
D | CO2(HCl) | 饱和碳酸氢钠溶液 | 洗气 |