题目内容
(2011?东城区模拟)已知物质M由同一短周期的X、Y两种元素组成,X原子的最外层电子数是最内层电子数的一半,Y元素最高正价与它的负价代数和为6.M与其他物质的转化关系如下(部分产物已略去):
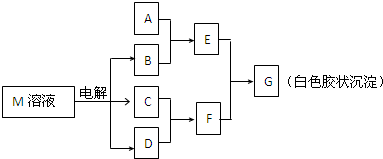
(1)工业电解M溶液的化学方程式为
(2)若A是X、Y同周期的一种常见金属,则A元素在周期表中的位置是
(3)若A是某元素的一种常见酸性氧化物,可用于制造光导纤维,则该元素原子结构示意图为
 ,写出E与F反应的离子方程式是
,写出E与F反应的离子方程式是
(4)B的电子式为: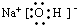
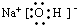 ,其中的化学键为:
,其中的化学键为:
(5)说明M物质的一种用途:

(1)工业电解M溶液的化学方程式为
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
.
| ||
(2)若A是X、Y同周期的一种常见金属,则A元素在周期表中的位置是
第三
第三
周期IIIA族
IIIA族
族,写出A与B溶液反应的化学方程式是2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
.(3)若A是某元素的一种常见酸性氧化物,可用于制造光导纤维,则该元素原子结构示意图为


2H++SiO32-=H2SiO3↓
2H++SiO32-=H2SiO3↓
.(4)B的电子式为:
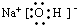
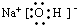
离子键和极性键
离子键和极性键
.(5)说明M物质的一种用途:
氯碱工业
氯碱工业
.分析:X、Y是短周期元素,X原子的最外层电子数是最内层电子数的一半,该元素可能是Li或Na元素,Y元素最高正价与它的负价代数和为6,最高正价与最低负价的绝对值是8,O元素没有正价,则Y是Cl元素,X和Y是同一周期元素,X是Na元素,Y是Cl元素,则M是NaCl;电解氯化钠溶液生成氢氧化钠、氯气和氢气;
(1)电解氯化钠溶液生成氢氧化钠、氯气和氢气;
(2)若A是X、Y同周期的一种常见金属,则A是金属Al,根据铝的电子层数和最外层电子数确定其在元素周期表中的位置,Al能和氢氧化钠溶液反应,所以B是氢氧化钠,氢氧化钠、铝和水反应生成偏铝酸钠和氢气;
(3)制造光导纤维的主要原料是二氧化硅,所以A是二氧化硅,二氧化硅能和氢氧化钠溶液反应生成硅酸钠和水,所以B是氢氧化钠,C和D反应生成氯化氢,硅酸钠和盐酸反应生成硅酸和氯化钠;
(4)根据离子化合物电子式的书写规则书写其电子式,氢氧化钠晶体中含有离子键和共价键;
(5)氯化钠可用于氯碱工业.
(1)电解氯化钠溶液生成氢氧化钠、氯气和氢气;
(2)若A是X、Y同周期的一种常见金属,则A是金属Al,根据铝的电子层数和最外层电子数确定其在元素周期表中的位置,Al能和氢氧化钠溶液反应,所以B是氢氧化钠,氢氧化钠、铝和水反应生成偏铝酸钠和氢气;
(3)制造光导纤维的主要原料是二氧化硅,所以A是二氧化硅,二氧化硅能和氢氧化钠溶液反应生成硅酸钠和水,所以B是氢氧化钠,C和D反应生成氯化氢,硅酸钠和盐酸反应生成硅酸和氯化钠;
(4)根据离子化合物电子式的书写规则书写其电子式,氢氧化钠晶体中含有离子键和共价键;
(5)氯化钠可用于氯碱工业.
解答:解:X、Y是短周期元素,X原子的最外层电子数是最内层电子数的一半,该元素可能是Li或Na元素,Y元素最高正价与它的负价代数和为6,最高正价与最低负价的绝对值是8,O元素没有正价,则Y是Cl元素,X和Y是同一周期元素,X是Na元素,Y是Cl元素,则M是NaCl;电解氯化钠溶液生成氢氧化钠、氯气和氢气;
(1)电解氯化钠溶液生成氢氧化钠、氯气和氢气,电解方程式为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑,
故答案为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑;
(2)若A是X、Y同周期的一种常见金属,则A是金属Al,铝原子核外有3个电子层,最外层有3个电子,所以其在周期表中处于第三周期、IIIA族,Al能和氢氧化钠溶液反应,所以B是氢氧化钠,氢氧化钠、铝和水反应生成偏铝酸钠和氢气,反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:第三周期、IIIA族,2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(3)制造光导纤维的主要原料是二氧化硅,所以A是二氧化硅,硅的原子结构示意图为 ,二氧化硅能和氢氧化钠溶液反应生成硅酸钠和水,所以B是氢氧化钠,C和D反应生成氯化氢,硅酸钠和盐酸反应生成硅酸和氯化钠,离子反应方程式为2H++SiO32-=H2SiO3↓,
,二氧化硅能和氢氧化钠溶液反应生成硅酸钠和水,所以B是氢氧化钠,C和D反应生成氯化氢,硅酸钠和盐酸反应生成硅酸和氯化钠,离子反应方程式为2H++SiO32-=H2SiO3↓,
故答案为: ;2H++SiO32-=H2SiO3↓;
;2H++SiO32-=H2SiO3↓;
(4)通过以上分析知,B是氢氧化钠,氢氧化钠电子式为: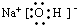 ,氢氧化钠中钠离子和氢氧根离子之间存在离子键,氧原子和氢原子之间存在极性共价键;
,氢氧化钠中钠离子和氢氧根离子之间存在离子键,氧原子和氢原子之间存在极性共价键;
故答案为: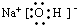 ;离子键和极性键;
;离子键和极性键;
(5)氯化钠可用于氯碱工业,故答案为:氯碱工业.
(1)电解氯化钠溶液生成氢氧化钠、氯气和氢气,电解方程式为:2NaCl+2H2O
| ||
故答案为:2NaCl+2H2O
| ||
(2)若A是X、Y同周期的一种常见金属,则A是金属Al,铝原子核外有3个电子层,最外层有3个电子,所以其在周期表中处于第三周期、IIIA族,Al能和氢氧化钠溶液反应,所以B是氢氧化钠,氢氧化钠、铝和水反应生成偏铝酸钠和氢气,反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:第三周期、IIIA族,2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(3)制造光导纤维的主要原料是二氧化硅,所以A是二氧化硅,硅的原子结构示意图为
 ,二氧化硅能和氢氧化钠溶液反应生成硅酸钠和水,所以B是氢氧化钠,C和D反应生成氯化氢,硅酸钠和盐酸反应生成硅酸和氯化钠,离子反应方程式为2H++SiO32-=H2SiO3↓,
,二氧化硅能和氢氧化钠溶液反应生成硅酸钠和水,所以B是氢氧化钠,C和D反应生成氯化氢,硅酸钠和盐酸反应生成硅酸和氯化钠,离子反应方程式为2H++SiO32-=H2SiO3↓,故答案为:
 ;2H++SiO32-=H2SiO3↓;
;2H++SiO32-=H2SiO3↓;(4)通过以上分析知,B是氢氧化钠,氢氧化钠电子式为:
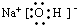 ,氢氧化钠中钠离子和氢氧根离子之间存在离子键,氧原子和氢原子之间存在极性共价键;
,氢氧化钠中钠离子和氢氧根离子之间存在离子键,氧原子和氢原子之间存在极性共价键;故答案为:
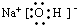 ;离子键和极性键;
;离子键和极性键;(5)氯化钠可用于氯碱工业,故答案为:氯碱工业.
点评:本题考查元素化合物的特性和反应,用框图设问可以考查学生正向思维、逆向思维、发散和收敛思维,能根据题眼正确判断化合物是解本题的关键,注意铝和氢氧化钠溶液的反应中,水作反应物,容易漏写,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目