题目内容
【题目】已知:(CH3COOH)2![]() 2CH3COOOH,实验测得不同压强下体系平均相对分子质量(
2CH3COOOH,实验测得不同压强下体系平均相对分子质量(![]() ) 随温度(T)变化曲线如图所示。下列说法正确的是
) 随温度(T)变化曲线如图所示。下列说法正确的是
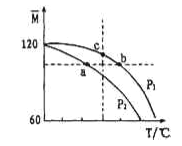
A. 该过程△H<0
B. 平衡常数:K (a) =K (b) <K (c)
C. 气体压强:p (a) <p (b) =p (c)
D. 当![]() =80时,n[(CH3COOH)2]:nCH3COOH =1: 1
=80时,n[(CH3COOH)2]:nCH3COOH =1: 1
【答案】C
【解析】A、根据反应方程式,反应物分子量大于生成物分子量,依据图像,随着温度的升高,平均分子量减少,说明反应向正反应方向进行,根据勒夏特列原理,正反应为吸热反应,即△H>0,故A错误;B、平衡常数只受温度的影响,此反应正反应是吸热反应,温度升高,平衡向正反应方向进行,平衡常数增大,即K(b)>K(c)>K(a),故B错误;C、增大压强,平衡向逆反应方向移动,平均摩尔质量增大,即P1>P2,有Pb=Pc>Pa,故C正确;D、假设开始时,通入(CH3COOH)2的物质的量为1mol,(CH3COOH)2![]() 2CH3COOOH
2CH3COOOH
起始: 1 0
变化: x 2x
某时刻:1-x 2x 根据平均摩尔质量的定义,则有M=![]() =80,解得x=0.5,(CH3COOH)2的物质的量为0.5mol,。CH3COOH的物质的量为1mol,故D错误。
=80,解得x=0.5,(CH3COOH)2的物质的量为0.5mol,。CH3COOH的物质的量为1mol,故D错误。

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
