题目内容
(1)1.2g RSO4中含0.01mol R2+,则RSO4的摩尔质量是______;R的相对原子质量约是______.(2)病人输液用的葡萄糖注射液是葡萄糖(化学式为C6H12O6)的水溶液,其标签上的部分内容如图所示.利用标签所提供的信息,回答下列问题:
①该注射液中葡萄糖的质量分数为______;
②该注射液中葡萄糖的物质的量浓度为______.
(3)现有一瓶A和B的混合液,已知它们的性质如下表.
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g?cm-3 | 溶解性 |
| A | -11.5 | 198 | 1.11 | A、B互溶,且均易溶于水 |
| B | 17.9 | 290 | 1.26 |

【答案】分析:(1)根据摩尔质量计算公式求算;摩尔质量以g/mol单位时,数值上与相对原子质量相等;
(2)①由标签所提供的信息可知该注射液中葡萄糖的质量分数;
②由溶质的质量=溶液质量×质量分数,n= 、c=
、c= 来计算该注射液中葡萄糖的物质的量浓度;
来计算该注射液中葡萄糖的物质的量浓度;
(3)根据题干信息,可以采用蒸馏方法.
解答:解:(1)M(RSO4)=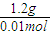 =120g/mol,摩尔质量以g/mol单位时,数值上与相对原子质量相等,
=120g/mol,摩尔质量以g/mol单位时,数值上与相对原子质量相等,
故答案是:120g/mol; 120;
(2)①由标签所提供的信息可知该注射液中葡萄糖的质量分数为5%,
故答案为:5%;
②溶质的质量为25g×5%=1.25g,n= =0.0069mol,则c=
=0.0069mol,则c=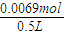 =0.01mol/L,
=0.01mol/L,
故答案为:0.01mol/L;
(3)A、B互溶,且均易溶于水,A、B的沸点差别比较大,可以采用蒸馏方法分离,
故答案是:蒸馏.
点评:本题考查了摩尔质量、质量分数、物质的量浓度的计算,本题难度中等.
(2)①由标签所提供的信息可知该注射液中葡萄糖的质量分数;
②由溶质的质量=溶液质量×质量分数,n=
 、c=
、c= 来计算该注射液中葡萄糖的物质的量浓度;
来计算该注射液中葡萄糖的物质的量浓度;(3)根据题干信息,可以采用蒸馏方法.
解答:解:(1)M(RSO4)=
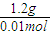 =120g/mol,摩尔质量以g/mol单位时,数值上与相对原子质量相等,
=120g/mol,摩尔质量以g/mol单位时,数值上与相对原子质量相等,故答案是:120g/mol; 120;
(2)①由标签所提供的信息可知该注射液中葡萄糖的质量分数为5%,
故答案为:5%;
②溶质的质量为25g×5%=1.25g,n=
 =0.0069mol,则c=
=0.0069mol,则c=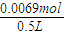 =0.01mol/L,
=0.01mol/L,故答案为:0.01mol/L;
(3)A、B互溶,且均易溶于水,A、B的沸点差别比较大,可以采用蒸馏方法分离,
故答案是:蒸馏.
点评:本题考查了摩尔质量、质量分数、物质的量浓度的计算,本题难度中等.

练习册系列答案
相关题目
 (1)1.2g RSO4中含0.01mol R2+,则RSO4的摩尔质量是______;R的相对原子质量约是______.
(1)1.2g RSO4中含0.01mol R2+,则RSO4的摩尔质量是______;R的相对原子质量约是______.
(2)病人输液用的葡萄糖注射液是葡萄糖(化学式为C6H12O6)的水溶液,其标签上的部分内容如图所示.利用标签所提供的信息,回答下列问题:
①该注射液中葡萄糖的质量分数为______;
②该注射液中葡萄糖的物质的量浓度为______.
(3)现有一瓶A和B的混合液,已知它们的性质如下表.
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g?cm-3 | 溶解性 |
| A | -11.5 | 198 | 1.11 | A、B互溶,且均易溶于水 |
| B | 17.9 | 290 | 1.26 |
 (1)1.2g RSO4中含0.01mol R2+,则RSO4的摩尔质量是
(1)1.2g RSO4中含0.01mol R2+,则RSO4的摩尔质量是