题目内容
【题目】利用如图所示装置(电极均为惰性电极)可吸收SO2,并用阴极排出的溶液吸收NO2。下列关于该装置的四种说法,正确的组合是
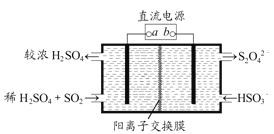
①.a为直流电源的负极
②.阴极的电极反应式为:2HSO3-+2H++2e-=S2O42-+2H2O
③.阳极的电极反应式为:SO2+2H2O-2e-=SO42-+4H+
④.电解时,H+由阴极室通过阳离子交换膜到阳极室
A. ①和② B. ①和③
C. ②和③ D. ③和④
【答案】C
【解析】由图中信息可知,两电极连接在直流电源上,所以该装置为电解池;二氧化硫被氧化为硫酸,而HSO3-被还原为S2O42-。根据电解原理,阳极上发生氧化反应而阴极上发生还原反应,所以通入二氧化硫的为阳极室,另一侧为阴极室,所以a连接电源的正极,①不正确,②和③是正确的;电解池中一般溶液中的阳离子向阴极定向移动,而阴离子向阳极定向移动,但是由于电解池使用了阳离子交换膜,所以只有阳离子H+才可以从阳极室通过阳离子交换膜向阴极室移动,④不正确。综上所述,C组合正确。

练习册系列答案
相关题目