题目内容
(4分)(2012?广东)下列应用不涉及氧化还原反应的是( )
| A.Na2O2用作呼吸面具的供氧剂 |
| B.工业上电解熔融状态的Al2O3制备Al |
| C.工业上利用合成氨实现人工固氮 |
| D.实验室用NH4Cl和Ca(OH)2制备NH3 |
D
氧化还原反应的本质特征是反应前后元素化合价的发生变化;依据元素化合价变化分析判断;
解:A、Na2O2用作呼吸面具的供氧剂,过氧化钠和二氧化碳反应生成碳酸钠和氧气,发生了氧化还原反应,故A不符合;
B、工业上电解熔融状态的Al2O3制备Al,是电解氧化铝发生氧化还原反应,故B不符合;
C、工业上利用合成氨实现人工固氮,是单质气体单质和氢气化合生成氨气,发生了氧化还原反应,故C不符合;
D、NH4Cl和Ca(OH)2制备NH3是复分解反应,故D符合;
故选D.
点评:本题考查了氧化还原反应的概念应用,本质特征化合价变化的判断,较简单.
解:A、Na2O2用作呼吸面具的供氧剂,过氧化钠和二氧化碳反应生成碳酸钠和氧气,发生了氧化还原反应,故A不符合;
B、工业上电解熔融状态的Al2O3制备Al,是电解氧化铝发生氧化还原反应,故B不符合;
C、工业上利用合成氨实现人工固氮,是单质气体单质和氢气化合生成氨气,发生了氧化还原反应,故C不符合;
D、NH4Cl和Ca(OH)2制备NH3是复分解反应,故D符合;
故选D.
点评:本题考查了氧化还原反应的概念应用,本质特征化合价变化的判断,较简单.

练习册系列答案
相关题目
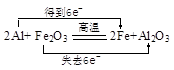
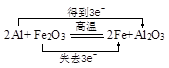
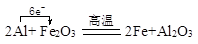
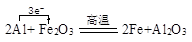
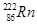 ,其原子中的质子数为136
,其原子中的质子数为136