题目内容
某溶液中含有下列六种离子:①HCO3-②SO32-③Na+④CO32-⑤NH4+⑥NO3-⑦SO42-向其中加入一定量Na2O2后,溶液中离子浓度基本保持不变的是( )
| A、①②⑤⑥ | B、③④⑤⑦ |
| C、②④⑦⑥ | D、只有⑥ |
考点:钠的重要化合物,离子共存问题
专题:离子反应专题,几种重要的金属及其化合物
分析:Na2O2与水反应生成NaOH和O2,反应后溶液成碱性,并且Na2O2具有强氧化性,凡是与NaOH或者与Na2O2发生氧化还原反应的离子浓度肯定发生变化,以此解答该题.
解答:
解:Na2O2与水反应生成NaOH和O2,反应后溶液成碱性,则:①HCO3-、④CO32-、⑤NH4+浓度发生变化,
Na2O2具有强氧化性,②SO32-被氧化生成SO42-,②SO32-⑦SO42-离子浓度发生变化,
③Na+浓度增大,
浓度不变的只有NO3-,
故选D.
Na2O2具有强氧化性,②SO32-被氧化生成SO42-,②SO32-⑦SO42-离子浓度发生变化,
③Na+浓度增大,
浓度不变的只有NO3-,
故选D.
点评:本题考查过氧化钠的性质,为高频考点,侧重于元素化合物知识的综合理解和运用的考查,题目难度不大,注意过氧化钠与水反应的特点以及具有氧化性的性质,为解答该题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
石英玻璃的主要成分是( )
| A、Na2SiO3 |
| B、SiO2 |
| C、MgSiO3 |
| D、CaSiO3 |
 在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件下关于离子存在的说法中正确的是( )
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系.下列条件下关于离子存在的说法中正确的是( )| A、a点对应的溶液中大量存在:Na+、Ba2+、Fe3+、Cl- |
| B、b点对应的溶液中大量存在:NH4+、K+、I-、NO3- |
| C、c点对应的溶液中大量存在:Cu2+、Na+、Cl-、S2- |
| D、d点对应的溶液中大量存在:K+、AlO2-、ClO-、Cl- |
关于下列各图的叙述正确的是( )
A、 表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJ?mol-1 |
B、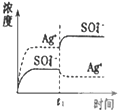 表示向Ag2SO4饱和溶液中加入等体积Na2SO4稀溶液,平衡会向左移动,Ksp减小 |
C、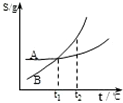 表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数B>A |
D、 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液 |
下列反应中Fe3+离子表现氧化性的是( )
| A、FeCl3溶液滴入沸水中,溶液变为红褐色 |
| B、FeCl3溶液中加入NaOH溶液产生红褐色沉淀 |
| C、FeCl3溶液中加入AgNO3溶液产生白色沉淀 |
| D、FeCl3溶液中通入H2S气体产生浅黄色S沉淀 |
已知两种弱酸HA、HB的电离平衡常数Ka(HA)>Ka(HB).下列有关说法正确的是( )
| A、等温浓度均为0.1mol?L-1的HA、HB溶液中,其溶液的pH大小为:pH(HA)>pH(HB) |
| B、在0.1mol?L-1的NaA溶液中各离子浓度关系为:c(Na+)>c(A-)>c(OH-)>c(H+) |
| C、等体积pH相同的HA、HB溶液,分别加入等浓度的NaOH溶液,恰好完全反应消耗的NaOH溶液体积HA比HB多 |
| D、等温浓度均为0.1mol?L-1的NaA、NaB溶液中,其溶液的pH大小为:pH(NaA)>pH(NaB) |
下列变化中,能一步实现的是( )
| A、SO2→H2SO3 |
| B、SiO2→H2SiO3 |
| C、NO2→HNO3 |
| D、S→SO3 |
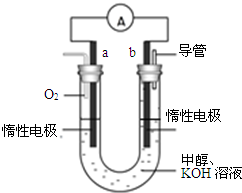 甲醇来源丰富.价格低廉.运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景.
甲醇来源丰富.价格低廉.运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景.