题目内容
【题目】等质量的两份铝分别放入过量盐酸和氢氧化钠溶液中,放出的氢气在相同状况下的体积比 ( )
A. 1:1 B. 1:6 C. 2:3 D. 3:2
【答案】A
【解析】试题分析:铝与足量的氢氧化钠溶液和稀盐酸分别发生反应:2Al+2H2O+2NaOH=2NaAlO2+3H2↑、2Al+6HCl=2AlCl3+3H2↑,若同温同压下放出相同体积的气体,选项A正确。故选A。

 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案【题目】甲醇是一种重要的有机化工原料。
(1)已知:
①C2H4(g)+H2O(g) ![]() C2H5OH(g) ΔH1=-45.5kJ/mol
C2H5OH(g) ΔH1=-45.5kJ/mol
②2CH3OH(g) ![]() CH3OCH3(g)+H2O(g) ΔH2=-23.9kJ/mol
CH3OCH3(g)+H2O(g) ΔH2=-23.9kJ/mol
③C2H4OH(g) ![]() CH3OCH3(g) ΔH3=+50.7kJ/mol
CH3OCH3(g) ΔH3=+50.7kJ/mol
请写出乙烯和水蒸气化合生成甲醇气体的热化学方程式:_____________。
(2)合成甲醇的反应为:CO(g)+2H2(g) ![]() CH3OH(g) ΔH。相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1:2的CO和H2的混合气体,改变温度进行实验,测得反应进行到t min时甲醇的体积分数如图甲所示。
CH3OH(g) ΔH。相同条件下,向容积相同的a、b、c、d、e五个密闭容器中分别充入等量的物质的量之比为1:2的CO和H2的混合气体,改变温度进行实验,测得反应进行到t min时甲醇的体积分数如图甲所示。
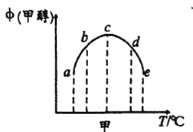
①温度升高甲醇的体积分数增大的原因是___________;
②根据图像判断ΔH________________(填“>”、“<”或“=”)0。
(3)某研究小组提出将4CH3OH+6NO2+8OH-=3N2+4CO32-+12H2O设计成原电池,以实现污染物的利用,装置如图乙所示(图中电极均为多孔的惰性电极)。
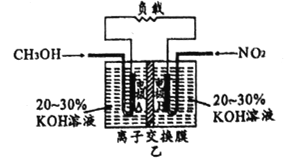
①电极A的名称是_____________。
②写出原电池电极B的电极反应式:___________。
③若用该电池对铁制品表面镀铜,反应一段时间后,铁制品质量增加64g,理论上处理NO2的质量为________g。
(4)为了研究甲醇转化为二甲醚的反应条件,某研究与小组在三个体积均为1.0L的恒容密闭容器中发生反应:2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ΔH2=-23.9KJ/mol。
CH3OCH3(g)+H2O(g) ΔH2=-23.9KJ/mol。
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
Ⅰ | T1 | 0.20 | 0.080 | 0.080 |
Ⅱ | T1 | 0.40 | a | a |
Ⅲ | T2 | 0.20 | 0.090 | 0.090 |
①T1温度下该反应的平衡常数K=_______;反应温度T1_________T2(填“大于”或“小于”。)
②容器Ⅱ中a=______。
③下列说法能说明反应达到平衡状态的是___________(填字母)。
A.容器中气体压强不再变化
B.用CH3OH 和CH3OCH3表示的反应速率之比为2:1
C.混合气体的密度不变
D.容器内CH3OH和CH3OCH3的浓度之比为2:1
E.单位时间内生成2molCH3OH 的同时生成1mol H2O(g)