题目内容
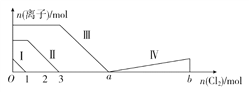
【题目】在含0.2 mol KOH和0.1 mol Ba(OH)2的混合溶液中持续通入6.72 L(标况)CO2的过程中,溶液中离子的物质的量n和通入CO2体积V的关系示意图正确的是( )
A.  B.
B. 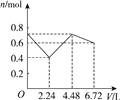
C. 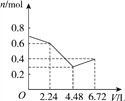 D.
D. 
【答案】A
【解析】二氧化碳的物质的量为0.3mol,混合溶液中的氢氧根离子物质的量为0.2+0.2=0.4mol,钾离子为0.2mol,钡离子为0.1mol,通入二氧化碳,二氧化碳和氢氧根离子反应生成碳酸根离子和水,碳酸根离子和钡离子反应生成碳酸钡沉淀,当通入0.1mol二氧化碳时,正好生成0.1mol碳酸钡沉淀,溶液还剩下0.2mol钾离子和0.2mol氢氧根离子,再通入二氧化碳,二氧化碳可以和氢氧根离子反应生成碳酸根离子,溶液中剩余的离子为0.2mol钾离子和0.1mol碳酸根离子,接着再通入0.1mol二氧化碳,与碳酸根离子反应生成碳酸氢根离子,溶液中含有0.2mol钾离子和0.2mol碳酸氢根离子,所以A图像符合题意。
故答案为A。

练习册系列答案
相关题目
【题目】在一定条件下,N2O分解的部分实验数据如下( )
反应时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
c(N2O)/molL-1 | 0.100 | 0.090 | 0.080 | 0.070 | 0.060 | 0.050 | 0.040 | 0.030 | 0.020 | 0.010 | 0.000 |
下图能正确表示该反应有关物理量变化规律的是( )
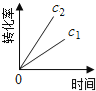
(注:图中半衰期指任一浓度N2O消耗一半时所需的相应时间,c1、c2均表示N2O初始浓度且c1<c2)
A. B.
B. C.
C. D.
D.