题目内容
| 高温 |

根据上述转化关系回答下列问题:
(1)写出A、D的结构简式:A:
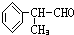
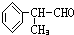
(2)D→E的反应类型为
(3)写山检验B中的官能团的试剂及出现的现象.
试剂
(4)写出C与E反应生成F的化学方程式


(5)“合成气”( CO、H2)除作合成有机物的原料外,还有其它用途,如
(6)F有多种同分异构体,写出满足下列条件的两种同分异构体的结构简式.
①属于酯类,且能发生银镜反应. ②苯环上的一氯取代物只有两种结构.
③分子结构中只有两个甲基.


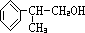 .C是甲酸,逆推可得,B是甲醛,A是甲醇.D和氢气发生加成反应生成E,所以D的结构简式为:
.C是甲酸,逆推可得,B是甲醛,A是甲醇.D和氢气发生加成反应生成E,所以D的结构简式为: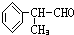 ,据此解答.
,据此解答.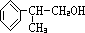 .C是甲酸,逆推可得,B是甲醛,A是甲醇.D和氢气发生加成反应生成E,所以D的结构简式为:
.C是甲酸,逆推可得,B是甲醛,A是甲醇.D和氢气发生加成反应生成E,所以D的结构简式为: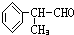 ,
,(1)由以上分析可知A为CH3OH,D为
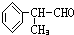 ,故答案为:CH3OH;
,故答案为:CH3OH;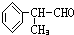 ;
;(2)D为
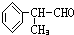 ,与氢气发生加成反应生成
,与氢气发生加成反应生成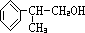 ;B为HCHO,含有醛基,故答案为:加成反应;醛基;
;B为HCHO,含有醛基,故答案为:加成反应;醛基;(3)B为HCHO,与新制氢氧化铜(或银氨溶液)产生砖红色沉淀(或产生光亮银镜),据此检验,
故答案为:新制氢氧化铜(或银氨溶液);产生砖红色沉淀(或产生光亮银镜);
(4)C为HCOOH,E为
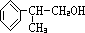 ,二者可在浓硫酸作用下发生酯化反应,反应的方程式为
,二者可在浓硫酸作用下发生酯化反应,反应的方程式为 ,
,故答案为:
 ;
;(5)“合成气”(CO、H2)除作合成有机物的原料外,还可以作燃料、合成氨等,故答案为:作燃料、合成氨等;
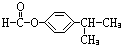
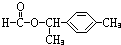
(6)F对应的同分异构体中①属于酯类,且能发生银镜反应,则应含有-OOCH结构,即为甲酸酯,②苯环上的一氯取代物只有两种结构,说明苯环结构对称,可能含有两个对位基团或三个基团,③分子结构中只有两个甲基.则对应的结构可能为:
 、
、 、
、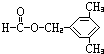 、
、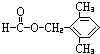 ,
,故答案为:
 ;
; 等.
等.
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
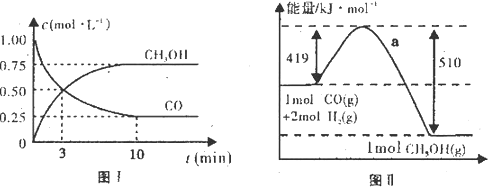
名师指导一卷通系列答案(19分)我国《车用燃料甲醇国家标准》的实施拉开了车用燃料低碳革命的大幕,一些省市正在陆续试点与推广使用甲醇汽油。甲醇可通过将煤的气化过程中生成的CO和H2在一定条件下发生如下反应制得:CO(g) + 2H2(g)  CH3OH(g)。图I、图Ⅱ是关于该反应进行情况的图示。
CH3OH(g)。图I、图Ⅱ是关于该反应进行情况的图示。

请根据图示回答下列问题:
(1)图I是反应时CO和CH3OH的浓度随时间的变化情况,从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=_______________。
(2)图Ⅱ表示该反应进行过程中能量的变化,曲线a表示不使用催化剂时反应的能量变化,在图Ⅱ中画出使用催化剂后的能量变化曲线b。
(3)写出该反应的热化学方程式 。
(4)该反应的平衡常数K的表达式为 ;当温度升高时,该平衡常数K将________(填“增大”、“减小”或“不变”)。
(5)恒容条件下,下列措施中能使 增大的有
。
增大的有
。
A.升高温度 B.充人He气
C.再充入1molCO和2molH2 D.使用催化剂
(6)在恒温条件下,保持CO浓度不变,扩大容器体积,则平衡 (填“逆向移动”、“正向移动”、“不移动”)
(7)在温度、容积相同的三个密闭容器中,按不同方式投料,保持恒温、恒容,测得反应达到平衡时的有关数据如下
|
容器 |
甲 |
乙 |
丙 |
|
投料量 |
1mol CO 、2mol H2 |
1molCH3OH |
2molCH3OH |
|
CH3OH的浓度(mol·L-1) |
c1 |
c2 |
c3 |
|
反应的能量变化 |
放出Q1 kJ |
吸收Q2 kJ |
吸收Q3 kJ |
|
体系压强(Pa) |
P1 |
P2 |
P3 |
|
反应物转化率 |
α1 |
α2 |
α3 |
则下列关系正确的是
A.c1= c2 B.Q3 = 2Q2 C.2 P1<P3
D.α1+α2=1 E.2α2=α3
E.2α2=α3
F.该反应若生成1molCH3OH放出的热量为(Q1+ Q2)kJ
(8)若在一体积可变的密闭容器中充入1mol CO、2mol H2和1molCH3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍,则该反应向 (填“正”、“逆”)反应方向移动,理由是

 时:
时:

 .
. ,已知在1100℃时,该反应的化学平衡常数K=0.263。
,已知在1100℃时,该反应的化学平衡常数K=0.263。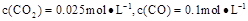 ,在这种情况下,该反应是否处于化学平衡状态? (填“是”或“否”),其判断依据是
。
,在这种情况下,该反应是否处于化学平衡状态? (填“是”或“否”),其判断依据是
。 来生产燃料甲醇,有关反应为:
来生产燃料甲醇,有关反应为: 。现向体积为1L的密闭容器中,充入1mol
。现向体积为1L的密闭容器中,充入1mol ,反应过程中测得
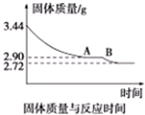
,反应过程中测得 (g)的浓度随时间的变化如图所示。
(g)的浓度随时间的变化如图所示。
 ;[来源:]
;[来源:] 增大的是 (填符号)。
增大的是 (填符号)。 (g)从体系中分离
E.充入He(g),使体系压强增大
(g)从体系中分离
E.充入He(g),使体系压强增大