题目内容
(6分)按要求写热化学方程式:
(1)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应生成正盐时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的热化学方程式_____________________。
(2)25℃、101 kPa条件下充分燃烧一定量的丁烷气体放出热量为Q kJ,经测定,将生成的CO2通入足量澄清石灰水中产生25 g白色沉淀,写出表示丁烷燃烧热的热化学方程式 。
(3)已知下列热化学方程式:
①CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
②C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ/mol
③H2(g)+O2(g)===H2O(l ) ΔH3=-285.8 kJ/mol
写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式 。
(1)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应生成正盐时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的热化学方程式_____________________。
(2)25℃、101 kPa条件下充分燃烧一定量的丁烷气体放出热量为Q kJ,经测定,将生成的CO2通入足量澄清石灰水中产生25 g白色沉淀,写出表示丁烷燃烧热的热化学方程式 。
(3)已知下列热化学方程式:
①CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
②C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ/mol
③H2(g)+O2(g)===H2O(l ) ΔH3=-285.8 kJ/mol
写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式 。
(1)H2SO4(aq)+NaOH(aq)===Na2SO4(aq)+H2O(l) ΔH=-57.3 kJ/mol(化学计量数、ΔH可成比例变化)
(2)C4H10(g)+O2(g)===4CO2(g)+5H2O(l) ΔH=-16Q kJ/mol
(3)2C(s)+2H2(g)+O2(g)===CH3COOH(l) ΔH=-488.3 kJ/mol
(2)C4H10(g)+O2(g)===4CO2(g)+5H2O(l) ΔH=-16Q kJ/mol
(3)2C(s)+2H2(g)+O2(g)===CH3COOH(l) ΔH=-488.3 kJ/mol
考查热化学方程式的书写。
(1)中和反应是放热反应,△H小于0,反应式为H2SO4(aq)+NaOH(aq)===Na2SO4(aq)+H2O(l) ΔH=-57.3 kJ/mol。
(2)25 g白色沉淀是碳酸钙,其物质的量是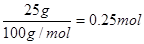 ,根据碳原子守恒可知,生成的CO2是0.25mol,则生成1molCO2放出的热量是4QkJ。燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,所以丁烷燃烧热的热化学方程式为C4H10(g)+O2(g)===4CO2(g)+5H2O(l) ΔH=-16Q kJ/mol。
,根据碳原子守恒可知,生成的CO2是0.25mol,则生成1molCO2放出的热量是4QkJ。燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,所以丁烷燃烧热的热化学方程式为C4H10(g)+O2(g)===4CO2(g)+5H2O(l) ΔH=-16Q kJ/mol。
(3)考查盖斯定律的应用和反应热的计算。将②×2+③×2-①,即得到2C(s)+2H2(g)+O2(g)===CH3COOH(l),所以反应热是-393.5kJ/mol×2-285.8 kJ/mol×2+870.3 kJ/mol=-488.3 kJ/mol。
(1)中和反应是放热反应,△H小于0,反应式为H2SO4(aq)+NaOH(aq)===Na2SO4(aq)+H2O(l) ΔH=-57.3 kJ/mol。
(2)25 g白色沉淀是碳酸钙,其物质的量是
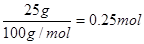 ,根据碳原子守恒可知,生成的CO2是0.25mol,则生成1molCO2放出的热量是4QkJ。燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,所以丁烷燃烧热的热化学方程式为C4H10(g)+O2(g)===4CO2(g)+5H2O(l) ΔH=-16Q kJ/mol。
,根据碳原子守恒可知,生成的CO2是0.25mol,则生成1molCO2放出的热量是4QkJ。燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,所以丁烷燃烧热的热化学方程式为C4H10(g)+O2(g)===4CO2(g)+5H2O(l) ΔH=-16Q kJ/mol。(3)考查盖斯定律的应用和反应热的计算。将②×2+③×2-①,即得到2C(s)+2H2(g)+O2(g)===CH3COOH(l),所以反应热是-393.5kJ/mol×2-285.8 kJ/mol×2+870.3 kJ/mol=-488.3 kJ/mol。

练习册系列答案
相关题目
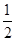 O2(g)=CO2(g)
O2(g)=CO2(g)  H=-283.0 kJ·mol-1
H=-283.0 kJ·mol-1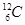 与
与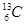 ;②O2与O3;③正丁烷和异丁烷;④金刚石和石墨;⑤冰与水;⑥CH3CH2OH和CH3OCH3;⑦H2与D2。
;②O2与O3;③正丁烷和异丁烷;④金刚石和石墨;⑤冰与水;⑥CH3CH2OH和CH3OCH3;⑦H2与D2。