题目内容
今有Na2CO3、NaHCO3、NaCl组成的混合物100g,加热到质量不再减少为止。剩余残渣为84.5g,将残渣溶于水,滴入足量的AgNO3溶液得到白色沉淀,加足量的稀硝酸后大部分沉淀消失,剩余沉淀为12.26g,试计算混合物中Na2CO3、NaHCO3、和NaCl的质量分数各是多少?
【答案】
53%、42%、5%
【解析】设NaHCO3的质量为X,Na2CO3的质量为Y
2NaHCO3 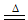 Na2CO3 +CO2 ↑+H2O
Na2CO3 +CO2 ↑+H2O
 168 62
168 62
X 100g-85.4g
列比例式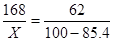 解之,X=42g
解之,X=42g
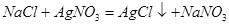
58.5 143.5
Y 12.26
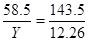 解之,Y=5g
解之,Y=5g
m(Na2CO3)=100-42-5=53g
由于混合物的总质量为100g,故混合物中Na2CO3、NaHCO3、和NaCl的质量分数分别为53%、42%、5%。

练习册系列答案
相关题目