题目内容
(1)浓硫酸与木炭粉在加热条件下反应的化学方程式是:_______________________。(2)试用图6-16所示各装置设计一个实验,来验证上述反应所产生的各种产物。

图6-16
这些装置的连接顺序(按产物气流从左至右的方向)是(填装置的编号):________→__________→_____________→_____________。
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用
是_______________________,B瓶溶液的作用是__________________,C瓶溶液的作用是___________________。
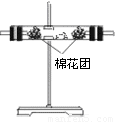
(4)装置②中所加固体的药品是___________,可验证的产物是_____________,确定装置②在整套装置中位置的理由_______________________________。
(5)装置③中所盛溶液是_________________,可验证的产物是__________________。
解析:(1)浓硫酸有氧化性,加热时氧化性更强,木炭粉有还原性,两者相互反应,浓硫酸被还原成SO2,木炭粉则被氧化成CO2,反应得到的三种气态产物是SO2、CO2和H2O。
(2)实验的目的是要将三种气态产物一一验证出来。由题中所给的各种装置可知:④是反应发生器;①中有品红溶液,可联想是用来验证SO2;装置③中装有某种水溶液,显然③可用来验证CO2;②是反应管,可验证水蒸气。由于①③中装的都是水溶液,气流经过后一定会带出水汽,所以必须先用②验证产物中的水蒸气,然后再验证SO2和CO2,不然就不能确证水蒸气一定是反应产物;由于SO2和CO2都能与石灰水反应,使澄清的石灰水变浑浊,因此从②出来的气体必须先经过①验证和除去SO2后再进入⑧验证CO2,由此可以得出正确的连接顺序应当是④②①③。
(3)A瓶中品红溶液褪色,可证明产物中有SO2,C瓶溶液不褪色说明进入C瓶的气体中已没有SO2,从而推断出B瓶的溶液作用是氧化吸收从A瓶出来的气体中全部SO2,因而C瓶溶液的作用是确认这时气流中SO2已被B瓶溶液全部吸收。
(4)因为②是验证水蒸气的,所以其中固体药品必是可与水结合,而且又可观察到明显现象变化的物质,我们比较熟悉的是白色无水硫酸铜遇水变蓝,或变色硅胶遇水由蓝色变粉红色。确定②装置位置的理由如(2)中所述。
(5)由于从①中C瓶出来的气流中已确证没有SO2,因此③中所盛溶液必定是澄清石灰水,用来验证气流中的CO2。
答案:(1)2H2SO4(浓)+C![]() CO2↑+2H2O+2SO2↑
CO2↑+2H2O+2SO2↑
(2)④ ② ① ③
(3)验证产物气流中有SO2 将产物气流中SO2全部氧化吸收 确认产物气流中SO2已被B瓶溶液全部吸收
(4)无水硫酸铜(或变色硅胶) 水蒸气 由于产物气流通过①③时会带出水蒸气,所以②必须在①③之前
(5)澄清石灰水 CO2

)(1)浓硫酸与木炭粉在加热条件下反应的化学方程式是:_____________________。
(2)试用下图所列各装置设计一个实验,来验证上述反应所产生的各种产物。
| 编号 | ① | ② | ③ | ④ |
| 装置 |
|
|
|
|
这些装置的连接顺序(按产物气流从左至右的方向)是(填装置的编号):____→____→_____→______。
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是______________,B瓶溶液的作用是_________________,C瓶溶液的作用是________________________。
(4)装置②中所加固体药品是______________,可验证的产物是______________,确定装置②在整套装置中位置的理由是_______________________________。
(5)装置③中所盛溶液是____________,可验证的产物是____________。
)(1)浓硫酸与木炭粉在加热条件下反应的化学方程式是:_____________________。
(2)试用下图所列各装置设计一个实验,来验证上述反应所产生的各种产物。
| 编号 | ① | ② | ③ | ④ |
| 装置 | | | | |
这些装置的连接顺序(按产物气流从左至右的方向)是(填装置的编号):____→____→_____→______。
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是______________,B瓶溶液的作用是_________________,C瓶溶液的作用是________________________。
(4)装置②中所加固体药品是______________,可验证的产物是______________,确定装置②在整套装置中位置的理由是_______________________________。
(5)装置③中所盛溶液是____________,可验证的产物是____________。
)(1)浓硫酸与木炭粉在加热条件下反应的化学方程式是:_____________________。
(2)试用下图所列各装置设计一个实验,来验证上述反应所产生的各种产物。
|
编号 |
① |
② |
③ |
④ |
|
装置 |
|
|
|
|
这些装置的连接顺序(按产物气流从左至右的方向)是(填装置的编号):____→____→_____→______。
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是______________,B瓶溶液的作用是_________________,C瓶溶液的作用是________________________。
(4)装置②中所加固体药品是______________,可验证的产物是______________,确定装置②在整套装置中位置的理由是_______________________________。
(5)装置③中所盛溶液是____________,可验证的产物是____________。



 →这些装置的连接顺序(按产物气流从左至右的方向)是(填装置的编号): →
→ →
。→
→这些装置的连接顺序(按产物气流从左至右的方向)是(填装置的编号): →
→ →
。→