题目内容
(14分)乙酰水杨酸(AsPirin)是一种常用的解热镇痛、抗风湿类药物,广泛应用于临床治疗和预防心脑血管疾病,近年来还不断发现它的新用途。乙酰水杨酸是一种有机弱酸,pKa=3.5,其结构式为:![]() ,易溶于乙醇而微溶于水。
,易溶于乙醇而微溶于水。
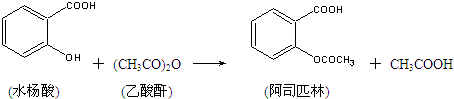
4-1 乙酰水杨酸可由水杨酸和乙酸酐反应得到,写出化学方程式;
4-2 估算0.1mol/L乙酰水杨酸溶液与0.1mol/L乙酰水杨酸钠盐溶液的pH;
4-3 乙酰水杨酸的含量可用NaOH标准溶液直接滴定。准确称取乙酰水杨酸0.25g,置于250mL锥形瓶中,加入25mL 溶液,摇动使其溶解,再向其中加入适量酚酞指示剂,用c(NaOH)mol/L的标准NaOH溶液滴定至 为终点,记录所消耗NaOH溶液的体积V(NaOH) mL。
(1)填写上面2个空格
(2)列出计算乙酰水杨酸的质量分数(%)的表达式。
4-4 如果再提供标准的盐酸溶液,请设计另一个实验,测定乙酰水杨酸的质量分数(%)。
(1)简要写出实验步骤(参考第3题的实验步骤)
(2)写出全部反应方程式;
(3)列出计算乙酰水杨酸的质量分数(%)的表达式。
4-1  (2分)
(2分)
4-2 2.3 8.2(各1分)
4-3 (1)95%乙醇(1分) 出现微红色,30秒钟不变色(1分)
(2)[0.1802 c(NaOH)V(NaOH) / 0.25]×100%(1分)
4-4 (1)准确称取乙酰水杨酸0.25g,加入c(NaOH)mol/L V(NaOH)mL(过量)的NaOH标准溶液,于水浴上加热使乙酰基水解完全后,再用c(HCl)mol/L HCl标准溶液回滴,以酚酞为指示剂,至酚酞红色腿去,耗去HCl溶液V(HCl)mL。(2分)
(2) +3OH-→
+3OH-→![]() +CH3COOH+2H2O(1分)
+CH3COOH+2H2O(1分)
![]() +H+→
+H+→![]() (1分) OH-+H+= H2O (1分)
(1分) OH-+H+= H2O (1分)
(3)0.1802 [c(NaOH)V(NaOH)-c(HCl)V(HCl)] / (2×0.25)×100%(2分)

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
| A、4-甲基水杨酸和邻甲基水杨酸的化学性质相同 | B、水杨酸中的所有原子可能共平面 | C、上述四种有机物中都不存在手性碳原子 | D、1mol水杨酸和1mol乙酰水杨酸分别与NaOH反应,最多都消耗2molNaOH |