题目内容
已知氧化还原反应:KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O
其中1 mol氧化剂在反应中得到的电子为
- A.6 mol
- B.5 mol
- C.3 mol
- D.4 mol
B
试题分析:根据KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O可以知道KClO3为氧化剂,且KClO3中的Cl的化学价为+5,,反应后变为0价,所以1 mol氧化剂在反应中得到的电子为5mol,故本题的答案为B。
考点:氧化还原反应
点评:本题考查了氧化还原反应,氧化还原反应是高考考查的重点和难点,本题部分学生很容易选择A选项,原因是不知道KClO3中的Cl的化学价转化为氯气中的氯。(氧化还原反应中元素的价态在邻价之间比较容易进行)
试题分析:根据KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O可以知道KClO3为氧化剂,且KClO3中的Cl的化学价为+5,,反应后变为0价,所以1 mol氧化剂在反应中得到的电子为5mol,故本题的答案为B。
考点:氧化还原反应
点评:本题考查了氧化还原反应,氧化还原反应是高考考查的重点和难点,本题部分学生很容易选择A选项,原因是不知道KClO3中的Cl的化学价转化为氯气中的氯。(氧化还原反应中元素的价态在邻价之间比较容易进行)

练习册系列答案
相关题目
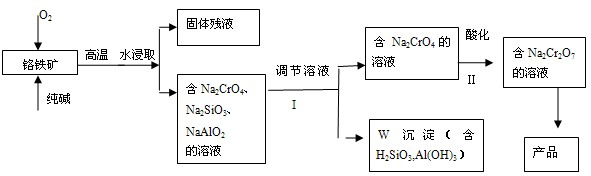
 化学科学的重要责任在于认识自然界里存在的各种各样的、奇妙的化学反应,探索纷繁的化学反应的本质和规律.通过化学反应原理模块的学习,我们可以比较深刻地理解化学科学的精髓,提高化学学科素养.请根据所学化学反应原理,解决以下问题.
化学科学的重要责任在于认识自然界里存在的各种各样的、奇妙的化学反应,探索纷繁的化学反应的本质和规律.通过化学反应原理模块的学习,我们可以比较深刻地理解化学科学的精髓,提高化学学科素养.请根据所学化学反应原理,解决以下问题.