题目内容
【题目】过氧化钠在供氧、防腐、除臭、微量分析等多方面有着重要用途,工业生产过氧化钠的方法是将除去二氧化碳且干燥后的空气通入熔融的钠(温度180~200℃)中得到氧化钠,然后增加空气流量并迅速升高温度至300~400℃即可得到过氧化钠。某化学兴趣小组模拟工业流程制备过氧化钠的装置如图所示。
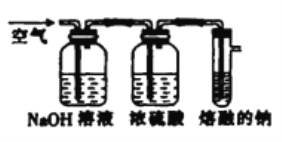
请回答下列相关问题。
(1)浓硫酸的作用是______________。
(2)升温至300~400℃时发生主要反应的化学方程式是______________。
(3)下列选项中的加热方式适合该实验的是_____(填字母)。
A.水浴 B.油裕(100~260℃) C.控温电炉(150~500℃) D.酒精喷灯(1000~1200℃)
(4)若要提高产品纯度,需在具支试管后添加一个装置,该装置应该是________。
(5)在具支试管后添加(4)中所要求的装置后,某同学还认为制得的过氧化钠中还含有少量的某种杂质,该杂质是________(填化学式)。
【答案】 干燥空气(或干燥氧气) 2Na2O+O2=2Na2O2 C 装有碱石灰的干燥管 Na3N
【解析】(1)参加反应的氧气必须是干燥的,所以浓硫酸的作用是干燥空气。(2)升温至300~400时发生的主要反应是氧化钠与氧气反应,反应的化学方程式是2Na2O+O2![]() 2Na2O2。(3)A.水浴的最高温度是100℃,低于300℃,A错误;B.油裕(100~260)温度低于300℃,B错误;C.控温电炉(150~500℃)可以使温度达到300~400℃,C正确;D.酒精喷灯(1000~1200℃)的温度太高,D错误,答案选C。(4)由于过氧化钠能与水或二氧化碳反应,所以若要提高产品纯度需要防止空气中的水蒸气和二氧化碳进入,因此需在具支试管后添加一个装置,该装置应该是装有碱石灰的干燥管。(5)由于空气中还含有氮气,氮气能与钠反应生成氮化钠,因此该杂质是Na3N。
2Na2O2。(3)A.水浴的最高温度是100℃,低于300℃,A错误;B.油裕(100~260)温度低于300℃,B错误;C.控温电炉(150~500℃)可以使温度达到300~400℃,C正确;D.酒精喷灯(1000~1200℃)的温度太高,D错误,答案选C。(4)由于过氧化钠能与水或二氧化碳反应,所以若要提高产品纯度需要防止空气中的水蒸气和二氧化碳进入,因此需在具支试管后添加一个装置,该装置应该是装有碱石灰的干燥管。(5)由于空气中还含有氮气,氮气能与钠反应生成氮化钠,因此该杂质是Na3N。

