题目内容
某金属氯化物MCl2 40.5g,含有0.6mol Cl-,则金属M的摩尔质量为
- A.135
- B.135g?mol-1
- C.64
- D.64g?mol-1
D
分析:由Cl-的物质的量,结合化学式MCl2计算金属氯化物的物质的量,再利用M=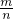 计算金属氯化物MCl2的摩尔质量,据此计算金属R的摩尔质量.
计算金属氯化物MCl2的摩尔质量,据此计算金属R的摩尔质量.
解答:因某金属氯化物MCl2中的Cl-的物质的量0.6mol,则MCl2的物质的量为0.3mol,
所以MCl2的摩尔质量为 =135g/mol,
=135g/mol,
所以金属M的摩尔质量为135g/mol-35.5mol×2=64g/mol.
故选D.
点评:本题考查摩尔质量的计算,难度较小,明确质量、摩尔质量、物质的量的关系即可解答.
分析:由Cl-的物质的量,结合化学式MCl2计算金属氯化物的物质的量,再利用M=
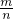 计算金属氯化物MCl2的摩尔质量,据此计算金属R的摩尔质量.
计算金属氯化物MCl2的摩尔质量,据此计算金属R的摩尔质量.解答:因某金属氯化物MCl2中的Cl-的物质的量0.6mol,则MCl2的物质的量为0.3mol,
所以MCl2的摩尔质量为
 =135g/mol,
=135g/mol,所以金属M的摩尔质量为135g/mol-35.5mol×2=64g/mol.
故选D.
点评:本题考查摩尔质量的计算,难度较小,明确质量、摩尔质量、物质的量的关系即可解答.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目