题目内容
【化学——选修有机化学基础】
下图中 A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物。
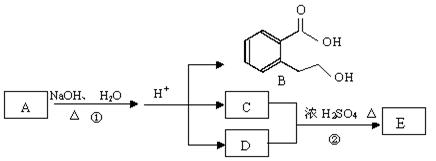
根据上图回答问题:
(1)已知E的相对分子质量为102,其中碳、氢两种元素的质量分数分别为58.8%、9.8%,其余为氧,则E的分子式为 。
(2)化合物B不能发生的反应是 (填字母序号):
a.加成反应 b.取代反应 c.消去反应 d.酯化反应 e.水解反应 f.置换反应
(3)反应②的化学方程式是 。
(4)C分子中的官能团名称是 ;A的结构简式是 。
(5)同时符合下列三个条件的B的同分异构体的数目有 个。
Ⅰ.含有间二取代苯环结构 Ⅱ.属于非芳香酸酯 Ⅲ.与 FeCl3溶液发生显色反应。写出其中任意一个同分异构体的结构简式 。
(15分)(1)C5H10O2 (2分) (2)e (2分)
(3)CH3COOH + CH3CH2CH2OH CH3COOCH2CH2CH3
+ H2O(2分)
CH3COOCH2CH2CH3
+ H2O(2分)
(4)羧基(1分);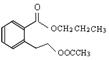 或
或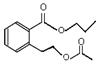 (2分)
(2分)
(5)4(2分) 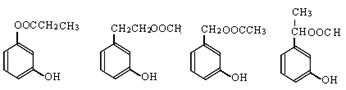 写出四者之一即可(2分)
写出四者之一即可(2分)
【解析】
试题分析:(1)E的相对分子质量为102,其中碳、氢两种元素的质量分数分别为58.8%、9.8%,则碳氢原子的个数分别是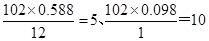 ,则氧原子的个数是
,则氧原子的个数是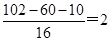 ,所以E的分子式为C5H10O2。
,所以E的分子式为C5H10O2。
(2)化合物B分子中含有羧基、羟基和苯环,所以不可能发生水解反应,答案选e。
(3)CD是A的水解产物,C和D的相对分子质量相等,且CD生成E,所以根据E的化学式可知,C、D分别是乙酸和丙醇,则该反应的化学方程式是CH3COOH
+ CH3CH2CH2OH CH3COOCH2CH2CH3
+ H2O。
CH3COOCH2CH2CH3
+ H2O。
(4)C分子中的官能团名称是羧基。根据BCD的结构简式可知,A的结构简式是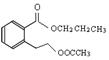 或
或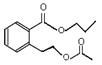 。
。
(5)与 FeCl3溶液发生显色反应,则分子中含有酚羟基。属于非芳香酸酯,这说明苯环上不存在羧基。又因为含有间二取代苯环结构,所以可能的结构简式是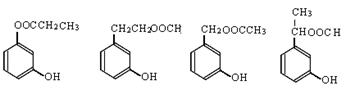 。
。
考点:考查有机物结构简式、化学式、性质以及同分异构体的判断和方程式的书写
点评:该题是高考中的常见题型,属于中等难度的试题。试题贴近高考,综合性强,在注重对基础知识巩固与训练的同时,侧重对学生能力的培养与解题方法的指导与训练。该类试题能较全面地考查学生的有机化学基础知识和逻辑思维能力、创造思维能力,提高学生的应试能力。该题的关键是记住常见官能团的结构、性质以及相互之间的转化,然后灵活运用即可。

 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案