题目内容
(10分)某化学兴趣小组在探究次氯酸钠溶液的性质时发现:
往过量FeSO4溶液中滴入几滴NaClO溶液,并加入适量硫酸,溶液立即变黄。
请你协助他们完成该反应还原产物的探究。
(1)甲同学推测该反应的还原产物为Cl2;乙同学推测该反应的还原产物为 。
(2)假设乙同学的推测是正确。
写出过量FeSO4溶液中,滴入几滴NaClO溶液,并加入适量硫酸的离子方程式:
。
请你设计一个实验方案,验证乙同学的推测是正确的。
要求在答题卡上按下表格式写出实验步骤、预期现象和结论(可以不填满):
往过量FeSO4溶液中滴入几滴NaClO溶液,并加入适量硫酸,溶液立即变黄。
请你协助他们完成该反应还原产物的探究。
(1)甲同学推测该反应的还原产物为Cl2;乙同学推测该反应的还原产物为 。
(2)假设乙同学的推测是正确。
写出过量FeSO4溶液中,滴入几滴NaClO溶液,并加入适量硫酸的离子方程式:
。
请你设计一个实验方案,验证乙同学的推测是正确的。
要求在答题卡上按下表格式写出实验步骤、预期现象和结论(可以不填满):
| 实验操作 | 预期现象和结论 |
| 步骤1:取上述反应后的溶液少许于试管A中, 。 | |
| 步骤2: 。 | |
| 步骤3: 。 | |
(10分)
(1)Cl-(2分)
(2)2Fe2+ + ClO-+ 2H+ = 2Fe3+ + Cl-+ H2O (2分)
SO42-、Cl-混合溶液中:要检验Cl-,排除SO42-干扰
(1)Cl-(2分)
(2)2Fe2+ + ClO-+ 2H+ = 2Fe3+ + Cl-+ H2O (2分)
SO42-、Cl-混合溶液中:要检验Cl-,排除SO42-干扰
| 实验步骤 | 预期现象和结论 |
| 步骤1:取上述反应后的溶液少许于试管A中,滴加过量Ba(NO3)2溶液,振荡、静置。(2分) | 有白色沉淀生成(1分) |
| 步骤2:取试管A中上层清液于试管B中,加稀HNO3酸化,加几滴AgNO3溶液。(2分) | 若有白色沉淀生成,乙同学的推测正确;(1分)。 |
(1)NaClO中氯元素为+1价,它的还原产物中氯的化合价无所谓为0价的氯气或—价的Cl-.
(2)本题考查了离子方程式的配平及离子的检验。
(2)本题考查了离子方程式的配平及离子的检验。

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目

 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑ 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑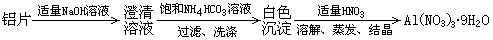 。
。