题目内容
下列说法错误的是( )
| A.金属镁着火,可用N2或CO2灭火 |
| B.MnO2、CuO、Fe三种物质的粉末都是黑色的,用稀盐酸可以将它们区别开 |
| C.用洁净的玻璃棒蘸取某物质灼烧时,焰色反应为黄色,则该物质不一定只含钠元素 |
| D.用氯水、KSCN溶液可以检验硫酸亚铁溶液中亚铁离子的存在 |
A、金属镁可以和氮气以及二氧化碳之间反应,金属镁着火,不可用N2或CO2灭火,故A错误;
B、MnO2、CuO、铁粉分别与浓盐酸反应的现象为:黄绿色气体生成、蓝色溶液、生成无色气体,现象不同,能区分开,故B正确;
C、用洁净的玻璃棒蘸取某物质灼烧时,焰色反应为黄色,则该物质不一定只含钠元素,还可能含有钾元素,故C正确;
D、检验硫酸亚铁溶液中亚铁离子的存在的方法:加入硫氰化钾,不变红,再加入氯水,会变红,证明含有亚铁离子,故D正确.
故选A.
B、MnO2、CuO、铁粉分别与浓盐酸反应的现象为:黄绿色气体生成、蓝色溶液、生成无色气体,现象不同,能区分开,故B正确;
C、用洁净的玻璃棒蘸取某物质灼烧时,焰色反应为黄色,则该物质不一定只含钠元素,还可能含有钾元素,故C正确;
D、检验硫酸亚铁溶液中亚铁离子的存在的方法:加入硫氰化钾,不变红,再加入氯水,会变红,证明含有亚铁离子,故D正确.
故选A.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
 、FeO、Fe2O3,Ti的最高化合价为+4)作原料,生产白色颜料二氧化钛的
、FeO、Fe2O3,Ti的最高化合价为+4)作原料,生产白色颜料二氧化钛的 主要步骤如下:
主要步骤如下: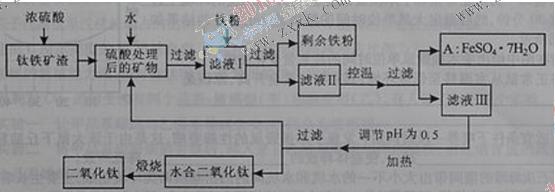
 色胶体中加入3336b kg A和112c kg铁粉,鼓入足量空气搅拌,反应完成后,有大量Fe2O3附着在胶体粒子上以沉淀形式析出;过滤后,沉淀经高温灼烧得红色颜料。若所得滤液中溶质只有硫酸钠和硫酸铁,则理论上可生产红色颜料_______________________kg。
色胶体中加入3336b kg A和112c kg铁粉,鼓入足量空气搅拌,反应完成后,有大量Fe2O3附着在胶体粒子上以沉淀形式析出;过滤后,沉淀经高温灼烧得红色颜料。若所得滤液中溶质只有硫酸钠和硫酸铁,则理论上可生产红色颜料_______________________kg。