题目内容
煤中含有硫元素,煤在燃烧过程中产生可引起酸雨的气体A。据有关部门监测,冬季平房区的空气中气体A的浓度明显升高。(1)气体A的名称是______。
(2)为降低气体A的排放量,人们采取了许多有力措施。措施之一是推广低硫煤,即通过向煤中加生石灰的方法,减少气体A的产生,此法称为“钙基固硫”。这种煤燃烧后大部分硫元素最终存在的形式为______。
A.CaS B.CaSO3 C.CaSO4 D.SO3
(3)若煤中硫含量(质量分数)为 0.32%,处理1000kg这种煤,至少应加入90%的生石灰______kg。
(4)在英国进行的一项研究结果表明,使用高烟囱可以有效地降低地表面气体A的浓度。在20世纪60年代,由火力发电厂排放出的气体A的浓度增加了35%,但由于建造高烟囱,地表面气体A的浓度降低了30%。从全球环境保护的角度分析这种方法是否可取,并说明所下结论的理由___________。
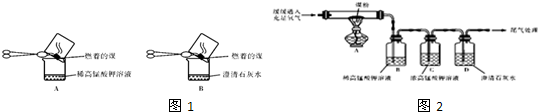
(5)在空气污染监测中,常用Br2与气体A的定量反应来测定空气中A的含量。写出水溶液中Br2与气体A反应的化学方程式 __________。
见解析
【试题分析】
(1)含硫煤的燃烧过程中,硫元素转化为SO2,SO2是引起酸雨的主要气体之一。
(2)向煤中加生石灰并燃烧,相关的化学方程式为2SO2+O2+2CaO=2CaSO4,所以最后硫元素主要以CaSO4形式被固定。故答案选C。
(3)这是一个典型的根据化学方程式计算的问题。因为煤中的硫元素的转化过程包括:S→SO2→CaSO4,所以有下列计算关系:
S ―― CaSO4 ―― CaO
32 56
1000×0.32% x×90%
故x=1000×0.32% ×56/( 32×90%)=6.22。
(4)加高烟囱只是使地表面SO2的浓度降低,没有减少SO2的实际排放量,且排放到高空中的SO2可被氧化为SO3,同样会形成酸雨,所以题述方法不可取。
(5)该反应充分利用了SO2的还原性和Br2的氧化性,其反应为:
SO2 + Br2 + 2H2O = H2SO4 + 2HBr

 名校课堂系列答案
名校课堂系列答案
“化学与技术”模块(10分)
煤中含有的硫元素主要以FeS2形式存在,煤在燃烧时,会产生大量的SO2,对环境产生污染,工业上有多种方法可以减少煤燃烧产生的SO2,这些方法可根据煤燃烧过程的不同阶段分成三类:
(1)在煤燃烧前采用的脱硫技术,其基本原理如下:
|
|
FeS2———————→ Fe2++SO![]() ———————→Fe3+
———————→Fe3+
这种脱硫技术称为 ① 脱硫技术,该技术的第一步反应的离子方程式为 ② ,第二步反应的离子方程式为 ③ 。煤炭中还有些硫元素是以有机物形式存在,人们正在利用微生物的降解作用,使之最终转化为 ④ 除去。
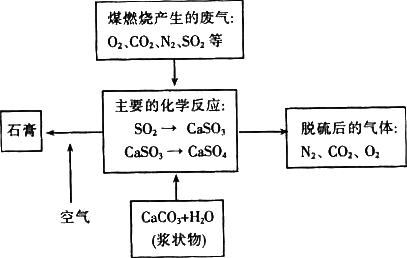
(2)在煤燃烧的同时进行的脱硫技术称为“流化床”燃烧技术,该技术是在煤中加入脱硫剂后直接在锅炉燃烧室燃烧,常用的脱硫剂是 ⑤ ,这种方法脱硫效率较高,且最终可得到脱硫副产品 ⑥ (写分子式)。
(3)在煤燃烧后,对其烟气净化技术,其基本原理是将烟气通入吸收塔进行除尘、脱硫、脱氮。吸收塔中常用的淋洗剂是 ⑦ ,这里所说的脱氮主要是指 ⑧ 这类物质。
“化学与技术”模块(10分)
煤中含有的硫元素主要以FeS2形式存在,煤在燃烧时,会产生大量的SO2,对环境产生污染,工业上有多种方法可以减少煤燃烧产生的SO2,这些方法可根据煤燃烧过程的不同阶段分成三类:
(1)在煤燃烧前采用的脱硫技术,其基本原理如下:
|
|
FeS2
———————→ Fe2++SO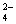 ———————→Fe3+
———————→Fe3+
这种脱硫技术称为 ① 脱硫技术,该技术的第一步反应的离子方程式为 ② ,第二步反应的离子方程式为 ③ 。煤炭中还有些硫元素是以有机物形式存在,人们正在利用微生物的降解作用,使之最终转化为 ④ 除去。
(2)在煤燃烧的同时进行的脱硫技术称为“流化床”燃烧技术,该技术是在煤中加入脱硫剂后直接在锅炉燃烧室燃烧,常用的脱硫剂是 ⑤ ,这种方法脱硫效率较高,且最终可得到脱硫副产品 ⑥ (写分子式)。
(3)在煤燃烧后,对其烟气净化技术,其基本原理是将烟气通入吸收塔进行除尘、脱硫、脱氮。吸收塔中常用的淋洗剂是 ⑦ ,这里所说的脱氮主要是指 ⑧ 这类物质 。