题目内容
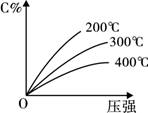
可逆反应mA(固)+nB(气) eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是(
)
eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是(
)

A.达平衡后,加入催化剂则C%增大
B.化学方程式中n>e+f
C.达平衡后,若升温,平衡右移
D.达平衡后,增加A的量有利于平衡向右移动
【答案】
B
【解析】
试题分析:A.达平衡后,加入催化剂化学平衡不发生移动。则C%不变。错误。B. 在温度不变的情况下,增大压强,C的含量升高。根据化学平衡移动原理。增大压强,化学平衡向气体体积减小的方向移动。即正反应方向是气体体积减小的反应。所以n>e+f.正确。C.在压强不变的情况下,升高温度C的含量降低。平衡向逆反应方向移动。由于升高温度,化学平衡向吸热反应方向移动。逆反应是吸热反应,则正反应是个放热反应。错误。D由于A是固体,当反应达到化学平衡后增加A的量平衡不会发生移动。错误。
考点:考查外界条件如温度、压强、催化剂、物质的量等对化学平衡的影响的知识。

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
可逆反应mA(固)+nB(气) eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图:下列叙述正确的是
eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图:下列叙述正确的是 
| A.达平衡后,加入催化剂则C%增大 |
| B.达平衡后,若升温,平衡左移 |
| C.化学方程式中n<e+f |
| D.达平衡后,增加A的量有利于平衡向右移动 |
可逆反应mA(固)+nB(气) eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度和压强的关系如右下图,下列叙述正确的是 ( )
eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度和压强的关系如右下图,下列叙述正确的是 ( )
| A.达平衡后,加入催化剂则C%增大 |
| B.达平衡后,若升温,平衡右移 |
| C.达平衡后,增加A的量有利于平衡向右移动 |
| D.化学方程式中n>e+f |
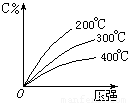
 eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是(
)
eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是(
)
 eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度和压强的关系如右下图,下列叙述正确的是 ( )
eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度和压强的关系如右下图,下列叙述正确的是 ( )