题目内容
我国是最早记载丹砂的药用价值和炼制方法的,为了使人们重视丹砂,1982年我国发行面值为10分的丹砂邮票.汞单质和化合物在工业生产和科学研究上有其广泛用途.丹砂炼汞的反应包括以下两个反应:
反应Ⅰ:HgS+O2
Hg+SO2
反应Ⅱ:4HgS+4CaO
4Hg+3CaS+CaSO4
请试完成下列各小题:
(1)HgS与氧气反应,氧化剂是
(2)请标出反应Ⅱ中电子转移的方向和目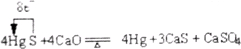
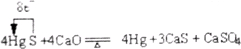 .
.
(3)得到的汞中含有铜等杂质,工业上常用5%的硝酸洗涤,写出除去少量铜杂质反应的离子方程式:
反应Ⅰ:HgS+O2
| ||
反应Ⅱ:4HgS+4CaO
| ||
请试完成下列各小题:
(1)HgS与氧气反应,氧化剂是
HgS和O2
HgS和O2
.(2)请标出反应Ⅱ中电子转移的方向和目
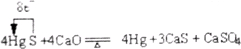
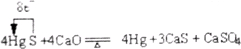
(3)得到的汞中含有铜等杂质,工业上常用5%的硝酸洗涤,写出除去少量铜杂质反应的离子方程式:
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.分析:(1)反应中Hg和O元素化合价降低,被还原,S元素化合价升高,被氧化;
(2)反应中Hg和S元素化合价发生变化,Hg元素化合价由+2价降低到0价,S元素部分升高到+6价,转移电子数为8;
(3)铜和稀硝酸反应生成硝酸铜、水和NO.
(2)反应中Hg和S元素化合价发生变化,Hg元素化合价由+2价降低到0价,S元素部分升高到+6价,转移电子数为8;
(3)铜和稀硝酸反应生成硝酸铜、水和NO.
解答:解:(1)反应中Hg和O元素化合价降低,被还原,S元素化合价升高,被氧化,则HgS既是氧化剂又是还原剂,氧气只起到氧化剂的作用,故答案为:HgS和O2;
(2)反应中Hg和S元素化合价发生变化,Hg元素化合价由+2价降低到0价,S元素部分升高到+6价,转移电子数为8,可表示为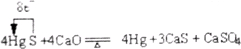 ,
,
故答案为: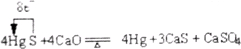 ;
;
(3)铜和稀硝酸反应生成硝酸铜、水和NO,反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,故答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O.
(2)反应中Hg和S元素化合价发生变化,Hg元素化合价由+2价降低到0价,S元素部分升高到+6价,转移电子数为8,可表示为
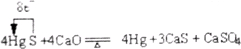 ,
,故答案为:
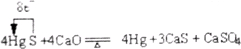 ;
;(3)铜和稀硝酸反应生成硝酸铜、水和NO,反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,故答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O.
点评:本题考查较为综合,涉及氧化还原反应知识,注意从元素化合价的角度判断相关概念和物质的表现出的性质,难度不大.

练习册系列答案
相关题目
| |||||||||||||||||||