��Ŀ����
����Ŀ������ѧ��ѡ��5���л���ѧ���������л���A�Ʊ��߷��ӻ�����F��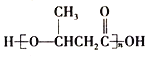 �����������£�
�����������£�
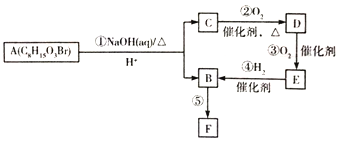
��ش��������⡣
��1��A�Ĺ�����������_______��C��ϵͳ������____________��
��2���ٵķ�Ӧ������_______���ݵķ�Ӧ������___________��
��3��д����Ӧ�۵Ļ�ѧ����ʽ��______________________��
��4����������������Bͬ���칹����____�֡�
��.����Na��Ӧ�������� ��.����NaOH ��Ӧ ��.������Na2CO3��Ӧ��
����NaOH��Һ��Ӧ���л����е�̼ԭ����ĿΪ2������ṹ��ʽ��__________��
��5����֪��
��. ![]()
��. 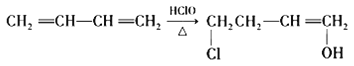
д����CH2=CHCH=CH2Ϊԭ���Ʊ�C�ĺϳ�·������ͼ�����Լ�������ѡ����__________��
���𰸡���ԭ�ӡ��ǻ������� 1��3-������ ȡ����Ӧ��ˮ�ⷴӦ ���۷�Ӧ 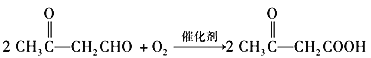 11 CH3COOCH2CH2OH��CH3COOCHOHCH3��CH3CH2OOCCH2OH
11 CH3COOCH2CH2OH��CH3COOCHOHCH3��CH3CH2OOCCH2OH 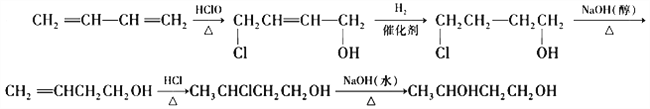
��������
����Aˮ������B��C��C����2���Ժ�����E��E�����������ӳɷ�Ӧ����B����B��C�����к�����ͬ��̼ԭ����������4����B�������۷�Ӧ����F�������F�Ľṹ��ʽ��֪B�Ľṹ��ʽΪHOCH(CH3)CH2COOH�����E�Ľṹ��ʽΪCH3COCH2COOH��D�Ľṹ��ʽΪCH3COCH2CHO�����C�Ľṹ��ʽΪCH3CHOHCH2CH2OH���ݴ˷�����𡣽�����Aˮ������B��C��C����2���Ժ�����E��E�����������ӳɷ�Ӧ����B����B��C�����к�����ͬ��̼ԭ����������4����B�������۷�Ӧ����F�������F�Ľṹ��ʽ��֪B�Ľṹ��ʽΪHOCH(CH3)CH2COOH�����E�Ľṹ��ʽΪCH3COCH2COOH��D�Ľṹ��ʽΪCH3COCH2CHO�����C�Ľṹ��ʽΪCH3CHOHCH2CH2OH����
��1��A�������࣬�Һ�����ԭ�Ӻ��ǻ������A�Ĺ�������������ԭ�ӡ��ǻ���������C�����к���2���ǻ�����ϵͳ������1��3-��������
��2���������Ϸ�����֪���ķ�Ӧ������ȡ����Ӧ��ˮ�ⷴӦ�����ķ�Ӧ���������۷�Ӧ��
��3����Ӧ����ȩ����������Ӧ����Ӧ�Ļ�ѧ����ʽΪ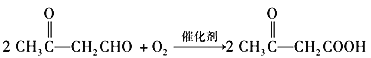 ��
��
��4����.����Na��Ӧ�������壬˵�������ǻ����Ȼ�����.����NaOH ��Ӧ��˵�������Ȼ�����������.������Na2CO3��Ӧ��˵�������������������Ȼ�������Ǽ����γɵ���������5�֣�����������γɵ�������2�֣�����ǻ�������Ҵ��γɵ�������1�֣������γɵ�������1�֣��ǻ�����ͼ״��γɵ�������2�֣�����11�֣�����NaOH��Һ��Ӧ���л����е�̼ԭ����ĿΪ2��������������л���ṹ��ʽ��CH3COOCH2CH2OH��CH3COOCHOHCH3��CH3CH2OOCCH2OH��
��5�������֪��Ϣ��������ʵĽṹ�����ʣ��������Ʒ���֪��ϳ�·�߿������Ϊ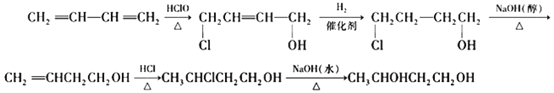 ��
��

����Ŀ��ij��ȤС���ö�п��Ƥ�����������Ʊ���ˮ������п(ZnSO4��7H2O)
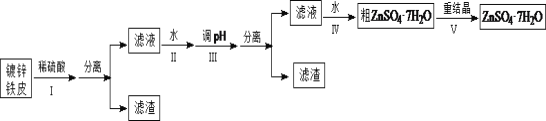
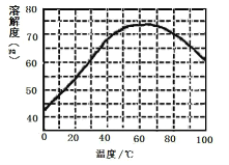
�����Ϣ���£��ٽ��������γ�����������������pH��Χ����ZnSO4���ܽ��(������100gˮ���ܽ������)���¶ȱ仯���ߡ�
�������� | pH | |
��ʼ���� | ��ȫ���� | |
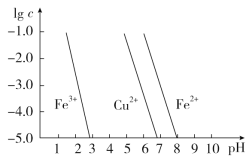
Fe3+ | 1.5 | 2.8 |
Fe2+ | 5.5 | 8.3 |
Zn2+ | 5.4 | 8.2 |
��ش�
(1)�ٶ�п��Ƥ�ϵ����ۿ���Na2CO3��Һȥ����������_______________________________���ڲ���������ж϶�п����ȫ��Ӧ��ʵ��������__________________________��
(2)�������������H2O2��������____(��������ɣ�����д����Ӧ�����ӷ�Ӧ����ʽ)��
(3)������ʵ�pH��Χ��____________________��
(4)���������Ҫ�õ���������������a.��������Һ���־�Ĥ��b.��60�������ܼ���c.��ȴ�����£�d.��100�������ܼ���e.���ˡ������������������ȷ˳��_____________(�������ظ�ʹ��)��
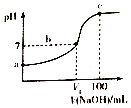
(5)�������ijͬѧ���ò�ͬ���·�ʽ������ȴ�ᾧ�����ZnSO4��7H2O���������С�ֲ���ͼ��ʾ�����ݸ�ʵ������Ϊ�˵õ�������С��Ծ�һ�Ľϴ�������ѡ��_______��ʽ������ȴ�ᾧ��
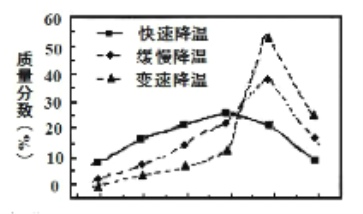
A. ���ٽ��� B. �������� C. ���ٽ���