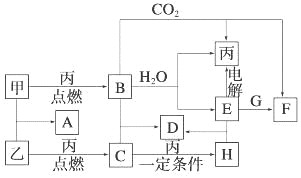
题目内容
【题目】(1)水(H2O)在很多化学反应中具有极其重要的作用。请研究下列水参与的氧化还原反应。 ①NaH+H2O=NaOH+H2↑
②2Na2O2+2H2O=4NaOH+O2↑
③2Na+2H2O =2NaOH+H2↑
④3NO2+H2O=2HNO3+NO
⑤2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
⑥2F2+2H2O=4HF+O2
水只作氧化剂的是____________;水只作还原剂的是____________;水既作氧化剂,又作还原剂的是____________;水既不作氧化剂,又不是还原剂的是____________。
(2)KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表示为:2KClO3+4HCl (浓)=2KCl+2ClO2↑+Cl2↑+2H2O。
①请分析该反应中电子转移的情况(用双线桥法表示)。
②浓盐酸在反应中显示出来的性质是________(填序号)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③若产生0.1 mol Cl2,则转移的电子的物质的量为________mol。
【答案】
(1)①③;⑥;⑤;②④
(2)①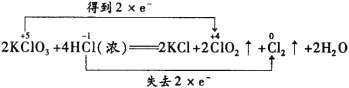
②B③0.2
【解析】
试题分析:
(1)氧化还原反应中,得到电子化合价降低的反应物是氧化剂,失去电子化合价升高的反应物是还原剂。①该反应中NaH中的H元素的化合价由-1价升高到0价,H2O中的H元素由+1降低到0价,所以氢化钠作还原剂,水作氧化剂; ②该反应中水中的H和O元素的化合价都不变,所以水既不是氧化剂又不是还原剂;③该反应中钠失电子化合价升高,水中氢元素化合价由+1价降低到0价,所以水作氧化剂;④该反应中,水中的H和O元素的化合价都不变,所以水既不是氧化剂又不是还原剂;⑤该反应中,水中氢元素的化合价由+1价降低到0价,水中氧元素的化合价由-2价升高到0价,所以水既是氧化剂又是还原剂;⑥该反应中,水中氧元素的化合价由-2价升高到0价,所以水作还原剂;所以水只作氧化剂的是①③;水只作还原剂的是⑥;水既作氧化剂,又作还原剂的是⑤;水既不作氧化剂,又不是还原剂的是②④。
(2)①反应2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2↑+2H2O中,部分HCl中氯元素化合价由-1价升高为Cl2中0价,KClO3中氯元素化合价由+5下降为ClO2中+4价,共转移2个电子,则反应中电子转移的双线桥法表示为 。
。
②反应中,部分HCl中氯元素化合价由-1价升高为Cl2中0价可知,HCl中氯元素被氧化,部分HCl转化为KCl,所以HCl在反应中还原剂与酸的作用,故B正确。
③反应中只有Cl2是氧化产物,HCl中氯元素化合价由-1价升高为Cl2中0价,所以产生0.1 mol Cl2,转移的电子的物质的量为0.1mol×2 =0.2mol。

【题目】化学在生活中有着广泛的应用,下列对应关系错误的是
化学性质 | 实际应用 | |
A | Al2(SO4)3和小苏打反应 | 泡沫灭火器灭火 |
B | 次氯酸盐具有氧化性 | 漂白粉漂白织物 |
C | HF与SiO2反应 | 氢氟酸在玻璃器皿上刻蚀标记 |
D | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
A. A B. B C. C D. D