题目内容
将nmol木炭粉和1mol氧化亚铁在反应器中混合,隔绝空气加强热。
⑴ 可能发生的化学反应有
① Fe+C=Fe+CO↑ ② 2FeO+C=2Fe+CO2↑ ③ FeO+CO=Fe+CO2↑
和④
⑵ 若n<1/4,充分反应后,反应器中的固体物质是 ,气体产物是 。
⑶ 若n<4,充分批应后,反应器中的固体物质是 ,气体产物是 。
⑷ 若反应的气体产物是混合物,n的取值范围是 。
⑸ 若反应的气体产物是混合物,且混合物中CO和CO2的物质的量相等,则n的值为 。
⑴ C+CO2 ![]() 2CO ⑵ FeO 和Fe,CO ⑶ C和Fe,CO ⑷ 1/2<n<1 ⑸ 2/3
2CO ⑵ FeO 和Fe,CO ⑶ C和Fe,CO ⑷ 1/2<n<1 ⑸ 2/3
解析:
解该题的思路首先从多种反应的特点出发,结合反应①和②得出:C和FeO的物质的量比大于或等于1∶1时,只生成CO;若比值是小于或等于1∶2时,只生成CO2。在1∶1和1∶2之间既有CO也有CO2生成。在数轴上可分为二点三区间:
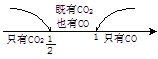
结合题意木炭和FeO的比值判断某一反应物是否过量,确定所发生的反应。再根据反应方程式的相加原理,简化计算步骤,最后应用范围讨论解法求解。
分析问题⑴中前三个方程式知C有还原性,CO2有一定的氧化性。既然题意是可能发生的反应,所以方程④是:C+CO2 ![]() 2CO。
2CO。
对于问题⑵,n<1/4,C和FeO物质的量之比是1∶4,说明FeO过量,所以,容器内的固体除产物Fe外,还应有FeO,而气体只有CO2。
对于问题⑶,C和FeO物质的量之比是4∶1,说明木炭过量。从反应区间知,经充分反应后,容器内的固体除产物Fe外, 还应有木炭,而气体只有CO。
对于问题⑷,气体产物是混合物,只能是CO和CO2,则固体物质只有Fe,根据前面的分析,n值应在1∶1和1∶2之间,即1/2<n<1,说明木炭既要参加①式反应,又要参加②式反应。
对于问题⑸,要求混合气体中CO和CO2物质的量相等,可将①式和②式按题意相加得:
3FeO+2C![]() 3Fe+CO↑+CO2↑,若FeO为1mol,则C为2/3。
3Fe+CO↑+CO2↑,若FeO为1mol,则C为2/3。

 ↑
↑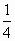 ,充分反应后,反应器中的固体物质是________,气体产物是________.
,充分反应后,反应器中的固体物质是________,气体产物是________.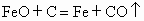 ;②
;②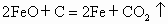 ;
;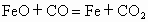 ;④___________________.
;④___________________.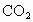 的物质的量相等,则n的值为_____________________.
的物质的量相等,则n的值为_____________________.