题目内容
NA表示阿伏加德罗常数的值,则关于热化学方程式:C2H2(g)+A.当10NA个电子转移时,该反应放出1 300 kJ的热量
B.当1NA个水分子生成且为液体时,吸收1 300 kJ的热量
C.当2 NA个碳氧共用电子对生成时,放出1 300 kJ的热量
D.当8 NA个碳氧共用电子对生成时,放出1 300 kJ的热量
解析: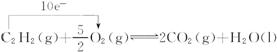 ΔH=-1 300 kJ·mol-1。当有10mol e-转移时,生成 1 mol 液态水,生成2 mol CO2(O=C=O),其中含8 mol碳氧共用电子对时,放出1 300 kJ的热量。
ΔH=-1 300 kJ·mol-1。当有10mol e-转移时,生成 1 mol 液态水,生成2 mol CO2(O=C=O),其中含8 mol碳氧共用电子对时,放出1 300 kJ的热量。
答案:AD

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目