题目内容
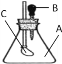
【题目】己知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量。该同学向pH=3.8酸化的、含有Fe2(SO4)3,杂质的CuSO4溶液中加入过量的黑色粉末X,充分搅拌后将滤液用下图所示装置电解,其中某电极增重ag,另一电极上产生标准状况下的气体VmL。下列说法正确的是( )

A. 铜电极连接电源正极 B. 铜的相对原子质量的计算式是![]()
C. 黑色粉末X是铁粉 D. 石墨电极上发生的反应是4OH--4e-=O2↑+2H2O
【答案】D
【解析】A.铜为电解池阴极,应连接电源负极,故A错误;B.设铜的相对原子质量为M,则n(Cu)=![]() mol=
mol=![]() mol,n(O2)=
mol,n(O2)=![]() =
=![]() mol,两极转移电子数目相等,则
mol,两极转移电子数目相等,则![]() mol×2=
mol×2=![]() mol×4,则M=
mol×4,则M=![]() ,故B错误;C.X为CuO,与酸反应调节溶液pH,可促进铁离子的水解而除去杂质,若加入铁粉,则能够将铜离子和铁离子还原,故C错误;D.石墨为阳极,电极上发生的反应是4OH--4e-=O2↑+2H2O,故D正确;故选D。
,故B错误;C.X为CuO,与酸反应调节溶液pH,可促进铁离子的水解而除去杂质,若加入铁粉,则能够将铜离子和铁离子还原,故C错误;D.石墨为阳极,电极上发生的反应是4OH--4e-=O2↑+2H2O,故D正确;故选D。

 名校课堂系列答案
名校课堂系列答案【题目】某含镍(Ni)废催化剂中主要含有Ni,还含有Al、Al2O3、Fe及其它不溶于酸、碱的杂质。部分金属氢氧化物Ksp近似值如下表所示:如下:
化学式 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 |
Ksp近似值 | 10-17 | 10-39 | 10-34 | 10-15 |
现用含镍废催化剂制备NiSO4·7H2O晶体,其流程图如下:

回答下列问题:
(1)“碱浸”时发生反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O,________________。
(2)“酸浸”所使用的酸为_____________。
(3)“净化除杂”需加入H2O2溶液,其作用是__________________________。然后调节pH使溶液中铁元素恰好完全沉淀,列式计算此时的pH。___________________________
(4)“操作A”为_____、过滤、洗涤、干燥,即得产品。
(5)NiSO4在强碱性溶液中可被NaClO氧化为NiOOH,该反应的离子方程式为__________________。
(6)NiOOH可作为镍氢电池的电极材料,该电池的工作原理如下图所示,其放电时,正极的电极反应式为__________________________________。