题目内容
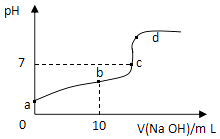
【题目】短周期主族元素X、Y、Z、W、R原子序数依次增大.m、p、r是这些元素组成的二元化合物,n、q、s是这些元素组成的三元化合物且属于离子化合物,其中s的水溶液俗称水玻璃,0.1mol/L n溶液的pH为13,m可制作耐火管且属于两性物质.上述物质的转化关系如图所示.下列说法正确的是( ) 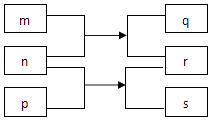
A.离子半径大小:Y>Z>W
B.简单气态氢化物的稳定性:R>Y
C.W的最高价氧化物对应的水化物碱性比Z的强
D.单质熔点:Z>R>X
【答案】A
【解析】解:s的水溶液俗称水玻璃,则s为Na2SiO3;m可制作耐火管且属于两性物质,则m为Al2O3;0.1mol/L n溶液的pH为13,则n为一元强碱溶液,应该为NaOH;结合短周期主族元素X、Y、Z、W、R原子序数依次增大可知,X为H、Y为O、Z为Na、W为Al、R为Si元素;n(NaOH)与p(Al2O3)反应生成r和q,且r是这些元素组成的二元化合物、q是这些元素组成的三元化合物,则r为H2O,q为NaAlO2;p是这些元素组成的二元化合物,p与n(NaOH)反应生成s(Na2SiO3)和r(H2O),则p为SiO2 , A.Y为O、Z为Na、W为Al,三种元素的离子具有相同的电子层,核电荷数越大,离子半径越小,则离子半径Y>Z>W,故A正确;
B.Y为O、R为Si元素,非金属性越强,氢化物稳定性越强,则对应氢化物的稳定性:Y>R,故B错误;
C.Z为Na、W为Al,金属性越强,最高价氧化物对应水合物的碱性越强,金属性Na>Al,则W的最高价氧化物对应的水化物碱性比Z的弱,故C错误;
D.X为H、Z为Na、R为Si,其单质分别为氢气、金属钠和硅,对应晶体分别为分子晶体、金属晶体和原子晶体,Si的沸点最高,氢气沸点最低,即单质沸点:R>Z>X,故D错误;
故选A.

 阅读快车系列答案
阅读快车系列答案【题目】甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上一般采用下列反应合成甲醇:
CO(g)+2H2(g)═CH3OH(g)△H1
①下表所列数据是反应在不同温度下的化学平衡常数(K).
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断△H10 (填“>”、“=”或“<”).
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为 , 此时的温度为(从上表中选择).