题目内容
【题目】下列叙述中错误的是( )
A.熔融状态下NaHSO4电离方程式为:NaHSO4(熔融)=Na++HSO![]() 。
。
B.强电解质的水溶液中无溶质分子,弱电解质的水溶液中有溶质分子
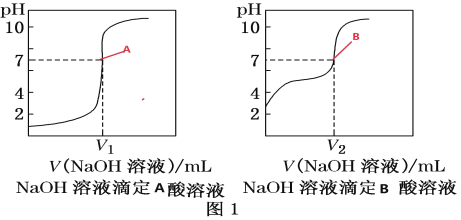
C.1 mol·L-1的醋酸溶液中c(H+)=0.01 mol·L-1可以证明醋酸是弱电解质
D.HF、HCl、BaSO4都是强电解质
【答案】D
【解析】
A.熔融状态下NaHSO4电离出钠离子和硫酸氢根离子,其电离方程式为:NaHSO4=Na++ HSO![]() ,故A正确,不选;
,故A正确,不选;
B.强电解质在水溶液中完全电离,所以溶液中无溶质分子,弱电解质在水溶液中不完全电离,所以弱电解质中有溶质分子,故B正确,不选;
C.1 mol·L-1的醋酸溶液中c(H+)=0.01 mol·L-1说明醋酸不完全电离,即醋酸为弱电解质,故C正确,不选;
D.HF为弱酸,是弱电解质,故D错误,符合题意;
故答案为D。

【题目】硅胶在干燥时因加有氯化钴(![]() )会有颜色的变化,随吸湿量的增加由蓝色逐渐转变成浅红色,使用非常方便。某学习小组设计实验制备氯化钴,并查阅到以下资料:钴与铁相似,常见化合价为+2、+3,可溶于稀盐酸(因反应极慢,需用硝酸作催化剂才可顺利进行)。钴在纯氧中加热至300℃以上生成CoO(熔点为1 935℃),400~900℃生成
)会有颜色的变化,随吸湿量的增加由蓝色逐渐转变成浅红色,使用非常方便。某学习小组设计实验制备氯化钴,并查阅到以下资料:钴与铁相似,常见化合价为+2、+3,可溶于稀盐酸(因反应极慢,需用硝酸作催化剂才可顺利进行)。钴在纯氧中加热至300℃以上生成CoO(熔点为1 935℃),400~900℃生成![]() 。请回答下列问题:
。请回答下列问题:
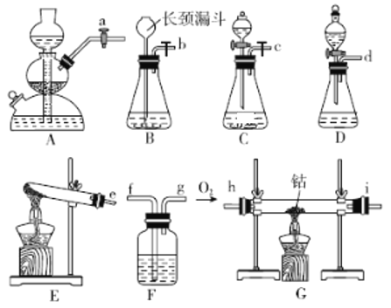
(1)实验①~④是制备氧气的试剂组合,请从A~E中选择最恰当装置符号填入表中。
实验 编号 | ① | ② | ③ | ④ |
试剂 | H2O2 溶液 | H2O2 溶液 | KMnO4 固体 | H2O2溶液 |
催化剂 | MnO2粉末 | FeCl3溶液 | 以Al2O3为载体,混有MnO2的块状物 | |
装置 | ____ | ____ | ______ | ______ |
(2)第一小组负责制备无水CoO,若选用装置C作为氧气的发生装置,则制备CoO完整装置的接口连接顺序为___________,装置C发生反应的化学方程式为_______;
(3)![]() 与
与![]() 类似,可以看作氧化钴(CoO)与氧化高钴(
类似,可以看作氧化钴(CoO)与氧化高钴(![]() )形成的化合物,写出
)形成的化合物,写出![]() 与盐酸反应的化学方程式:________________。
与盐酸反应的化学方程式:________________。
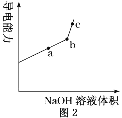
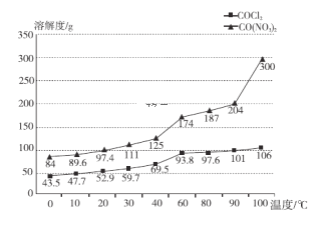
(4)第二小组同学提出另外的方案:用一定质量的钴粉与稀盐酸反应,滴入几滴稀硝酸,将得到的溶液倒入蒸发皿中,加热蒸发浓缩,38~40℃冷却结晶,趁热过滤,得到晶体。根据如图溶解度随温度变化,曲线解释能得到氯化钴晶体的原因:__________。
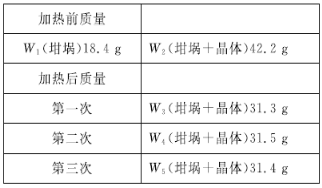
(5)为了确定晶体的化学式,小组同学把晶体洗涤、干燥、称量得到23.8 g固体,用坩埚加热至质量不再变化,数据如表所示,则该晶体的化学式为________。