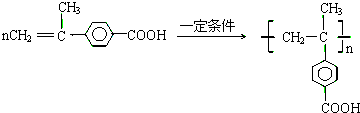
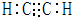题目内容
下列反应中,其放出热量的是
①NaOH溶液中加入盐酸
②由乙醇制C2H4
③铝热反应
④由氯酸钾制O2
- A.①②
- B.②③
- C.①③
- D.①④
C
①为中和反应属于放热反应;铝热反应有大量的热放出,属于放热反应;而②④在反应过程中均需要不断加热提供热量,均为吸热反应。
①为中和反应属于放热反应;铝热反应有大量的热放出,属于放热反应;而②④在反应过程中均需要不断加热提供热量,均为吸热反应。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列反应中,其放出热量的是
①NaOH溶液中加入盐酸 ②由乙醇制C2H4 ③铝热反应 ④由氯酸钾制O2
| A.①② | B.②③ | C.①③ | D.①④ |
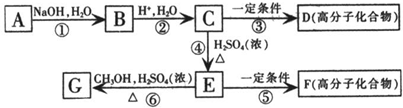
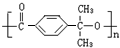
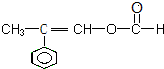
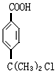 +2NaOH
+2NaOH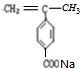 +NaCl+2H2O
+NaCl+2H2O