题目内容
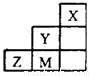
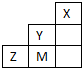 如图为短周期的一部分,推断关于Y、Z、M的说法正确的是( )
如图为短周期的一部分,推断关于Y、Z、M的说法正确的是( )分析:由元素在周期表中的相对位置可知,X为氦元素,Y为F元素,Z为S元素,M为Cl元素.
A、同周期随原子序数增大,非金属性增强,同主族自上而下非金属性减弱;
B、X为氦元素,单质属于稀有气体;
C、同周期随核电荷数增大,原子半径减小,同主族自上而下原子半径增大;
D、氟原子质子数为9,核外电子数为9,有2个电子层,最外层有7个电子.
A、同周期随原子序数增大,非金属性增强,同主族自上而下非金属性减弱;
B、X为氦元素,单质属于稀有气体;
C、同周期随核电荷数增大,原子半径减小,同主族自上而下原子半径增大;
D、氟原子质子数为9,核外电子数为9,有2个电子层,最外层有7个电子.
解答:解:由元素在周期表中的相对位置可知,X为氦元素,Y为F元素,Z为S元素,M为Cl元素.
A、同周期随原子序数增大,非金属性增强,所以非金属性M>Z,同主族自上而下非金属性减弱,所以非金属性Y>M,所以非金属性Y>M>Z,故A错误;
B、X为氦元素,属于稀有气体元素,故B正确;
C、同周期随核电荷数增大,原子半径减小,所以原子半径Z>M,同主族自上而下原子半径增大,所以原子半径M>Y,所以原子半径Z>M>Y,故C错误;
D、氟原子质子数为9,核外电子数为9,有2个电子层,最外层有7个电子,原子结构示意图为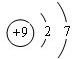 ,故D错误.
,故D错误.
故选:B.
A、同周期随原子序数增大,非金属性增强,所以非金属性M>Z,同主族自上而下非金属性减弱,所以非金属性Y>M,所以非金属性Y>M>Z,故A错误;
B、X为氦元素,属于稀有气体元素,故B正确;
C、同周期随核电荷数增大,原子半径减小,所以原子半径Z>M,同主族自上而下原子半径增大,所以原子半径M>Y,所以原子半径Z>M>Y,故C错误;
D、氟原子质子数为9,核外电子数为9,有2个电子层,最外层有7个电子,原子结构示意图为
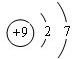 ,故D错误.
,故D错误.故选:B.
点评:本题考查元素周期表结构与元素周期律等,难度不大,整体把握周期表结构,关键是元素周期律的递变规律的掌握.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 (2013?珠海一模)如图为短周期的一部分,Y原子最外层电子数是其电子层数的2倍,下列说法正确的是( )
(2013?珠海一模)如图为短周期的一部分,Y原子最外层电子数是其电子层数的2倍,下列说法正确的是( )