题目内容
(2009?肇庆二模)W、X、Y、Z为同一短周期元素,原子序数依次增大.已知W、Y、Z三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水.下列判断正确的是( )
分析:W、X、Y、Z为同一短周期元素,原子序数依次增大,W、Y、Z三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水,则Y为Al,W为Na,X为Mg,而Z为Cl,以此来解答.
解答:解:W、X、Y、Z为同一短周期元素,原子序数依次增大,W、Y、Z三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水,则Y为Al,W为Na,X为Mg,而Z为Cl,
A.Z为S,则在第三周期ⅥA族,若Z为Cl,则在第三周期ⅤⅡA族,故A错误;
B.W为Na,Y为Al,Z为S或Cl,W、Y、Z三种元素中有两种金属、一种非金属,故B正确;
C.W、X、Y三种元素的单质中X为Mg,其最外层s电子为全满,稳定结构,熔沸点最大,故C错误;
D.W、Y、Z三种元素的最高价氧化物的水化物分别为NaOH、Al(OH)3、HClO4,分别为强碱、弱碱、强酸,故D错误;
故选B.
A.Z为S,则在第三周期ⅥA族,若Z为Cl,则在第三周期ⅤⅡA族,故A错误;
B.W为Na,Y为Al,Z为S或Cl,W、Y、Z三种元素中有两种金属、一种非金属,故B正确;
C.W、X、Y三种元素的单质中X为Mg,其最外层s电子为全满,稳定结构,熔沸点最大,故C错误;
D.W、Y、Z三种元素的最高价氧化物的水化物分别为NaOH、Al(OH)3、HClO4,分别为强碱、弱碱、强酸,故D错误;
故选B.
点评:本题考查位置、结构、性质,明确元素的推断是解答本题的关键,并熟悉元素及其化合物的性质来解答即可,题目难度不大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
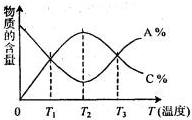 (2009?肇庆二模)经一定时间后,可逆反应aA+bB?cC中物质的含量A%和C%随温度的变化曲线如图所示.下列说法正确的是( )
(2009?肇庆二模)经一定时间后,可逆反应aA+bB?cC中物质的含量A%和C%随温度的变化曲线如图所示.下列说法正确的是( ) 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )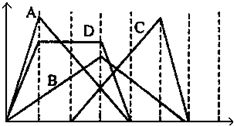 (2009?肇庆二模)下图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量.下列反应对应的曲线错误的是( )
(2009?肇庆二模)下图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量.下列反应对应的曲线错误的是( )