题目内容
在常温常压下,甲烷和足量O2的混合气体57 mL,点燃爆炸后,剩余气体为23 mL(恢复到原来状况时)。求原来甲烷的体积是多少?
17 mL或23 mL
CH4+2O2 CO2+2H2O
CO2+2H2O
H2O在常温常压时为液体,当有1体积CH4完全燃烧时气体体积减小2体积,
则V(CH4)= ="17" mL
="17" mL
反应消耗的O2的体积:V(O2)=2V(CH4)="34" mL
故原气体中CH4的体积可能为17 mL+(57 mL-17 mL-34 mL)="23" mL。
 CO2+2H2O
CO2+2H2OH2O在常温常压时为液体,当有1体积CH4完全燃烧时气体体积减小2体积,
则V(CH4)=
 ="17" mL
="17" mL反应消耗的O2的体积:V(O2)=2V(CH4)="34" mL
故原气体中CH4的体积可能为17 mL+(57 mL-17 mL-34 mL)="23" mL。

练习册系列答案
相关题目
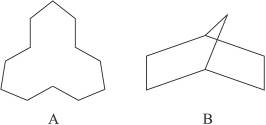
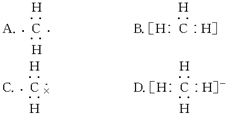
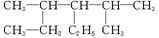 的物质,其名称是( )
的物质,其名称是( )