题目内容
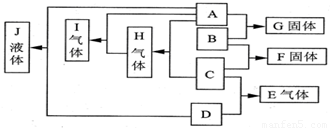
如图所示为短周期元素组成的中学常见A~J十种物质的转换关系.已知A、B、C、D均为单质,通常状况下只有A、C、D为气态.它们在一定条件下发生图示化学反应,得到E~J等化合物(图中物质的状态均为常温常压下).有关反应的化学计量数关系为:①A与B按物质的量之比n(A)/n(B)=1/2完全反应生成G;②B与C按物质的量之比n(B)/n(C)=3/1完全反应生成F;③C与D按物质的量之比n(C)/n(D)=1/3完全反应生成E.

请填空:
(1)G的电子式是______,其化学键类型是______;
(2)物质C反应后成F的化学方程式为______;
(3)实验室中制取E反应的化学方程式为______,干燥E时常用干燥剂的名称是______.
(4)常温下将F投入J中可生成E和一种白色难溶物X,该反应的化学方程式为______;若将I通入J中可生成H和某物质Y,X与Y溶液可发生中和反应,请写出前一反应的离子方程式为______.
解:A、D为气体单质,二者反应生成J为液态,则J应为H2O,而A和B反应生成固体,则A应为O2,D为H2,C与D按物质的量之比 =
=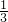 完全反应生成E,则E应为NH3,C为N2,所以H为NO,I为NO2,B与C按物质的量之比
完全反应生成E,则E应为NH3,C为N2,所以H为NO,I为NO2,B与C按物质的量之比 =
= ,完全反应生成F,则F应为Mg3N2,发生3Mg+N2
,完全反应生成F,则F应为Mg3N2,发生3Mg+N2 Mg3N2,则B为Mg,G为MgO,则
Mg3N2,则B为Mg,G为MgO,则
(1)G为MgO,为离子化合物,含有离子键,电子式为 ,故答案为:
,故答案为: ; 离子键;
; 离子键;
(2)C为N2,B为Mg,发生3Mg+N2 Mg3N2,故答案为:3Mg+N2
Mg3N2,故答案为:3Mg+N2 Mg3N2;
Mg3N2;
(3)实验室用氯化铵和熟石灰反应生成氨气,氨气为碱性气体,应用碱石灰干燥,反应的化学方程式为
2NH4Cl+Ca(OH)2 2NH3↑+2H2O+CaCl2,
2NH3↑+2H2O+CaCl2,
故答案为:2NH4Cl+Ca(OH)2 2NH3↑+2H2O+CaCl2; 碱石灰;
2NH3↑+2H2O+CaCl2; 碱石灰;
(4)Mg3N2和水反应生成Mg(OH)2和NH3,反应的化学方程式为Mg3N2+6H2O=3Mg(OH)2+2NH3↑,
NO2和水反应生成HNO3和NO,反应的离子方程式为3NO2+H2O=2H++2NO3-+NO,
故答案为:Mg3N2+6H2O=3Mg(OH)2+2NH3↑;3NO2+H2O=2H++2NO3-+NO.
分析:A、D为气体单质,二者反应生成J为液态,则J应为H2O,而A和B反应生成固体,则A应为O2,D为H2,C与D按物质的量之比 =
=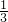 完全反应生成E,则E应为NH3,C为N2,所以H为NO,
完全反应生成E,则E应为NH3,C为N2,所以H为NO,
I为NO2,B与C按物质的量之比 =
= ,完全反应生成F,则F应为Mg3N2,发生3Mg+N2
,完全反应生成F,则F应为Mg3N2,发生3Mg+N2 Mg3N2,则B为Mg,G为MgO,结合物质的性质解答该题.
Mg3N2,则B为Mg,G为MgO,结合物质的性质解答该题.
点评:本题考查无机物的推断,题目难度较大,注意推断的突破口为A、D为气体单质,二者反应生成J为液态,则J应为H2O,根据物质反应的物质的量关系判断可能的反应.
 =
=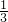 完全反应生成E,则E应为NH3,C为N2,所以H为NO,I为NO2,B与C按物质的量之比
完全反应生成E,则E应为NH3,C为N2,所以H为NO,I为NO2,B与C按物质的量之比 =
= ,完全反应生成F,则F应为Mg3N2,发生3Mg+N2
,完全反应生成F,则F应为Mg3N2,发生3Mg+N2 Mg3N2,则B为Mg,G为MgO,则
Mg3N2,则B为Mg,G为MgO,则(1)G为MgO,为离子化合物,含有离子键,电子式为
 ,故答案为:
,故答案为: ; 离子键;
; 离子键;(2)C为N2,B为Mg,发生3Mg+N2
 Mg3N2,故答案为:3Mg+N2
Mg3N2,故答案为:3Mg+N2 Mg3N2;
Mg3N2;(3)实验室用氯化铵和熟石灰反应生成氨气,氨气为碱性气体,应用碱石灰干燥,反应的化学方程式为
2NH4Cl+Ca(OH)2
 2NH3↑+2H2O+CaCl2,
2NH3↑+2H2O+CaCl2,故答案为:2NH4Cl+Ca(OH)2
 2NH3↑+2H2O+CaCl2; 碱石灰;
2NH3↑+2H2O+CaCl2; 碱石灰;(4)Mg3N2和水反应生成Mg(OH)2和NH3,反应的化学方程式为Mg3N2+6H2O=3Mg(OH)2+2NH3↑,
NO2和水反应生成HNO3和NO,反应的离子方程式为3NO2+H2O=2H++2NO3-+NO,
故答案为:Mg3N2+6H2O=3Mg(OH)2+2NH3↑;3NO2+H2O=2H++2NO3-+NO.
分析:A、D为气体单质,二者反应生成J为液态,则J应为H2O,而A和B反应生成固体,则A应为O2,D为H2,C与D按物质的量之比
 =
=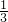 完全反应生成E,则E应为NH3,C为N2,所以H为NO,
完全反应生成E,则E应为NH3,C为N2,所以H为NO,I为NO2,B与C按物质的量之比
 =
= ,完全反应生成F,则F应为Mg3N2,发生3Mg+N2
,完全反应生成F,则F应为Mg3N2,发生3Mg+N2 Mg3N2,则B为Mg,G为MgO,结合物质的性质解答该题.
Mg3N2,则B为Mg,G为MgO,结合物质的性质解答该题.点评:本题考查无机物的推断,题目难度较大,注意推断的突破口为A、D为气体单质,二者反应生成J为液态,则J应为H2O,根据物质反应的物质的量关系判断可能的反应.

练习册系列答案
相关题目