题目内容
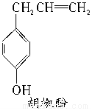
某有机物A遇FeCl3溶液显紫色,1molA最多能与3molNaOH反应。经测定,A的分子式为C8H8O3并且含有二取代苯结构,则A的结构式的数目为
A. 3 B. 4 C. 5 D. 6
练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
下列根据实验操作和现象得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 将少量Fe(NO3)2试样加水溶解后,滴 加稀硫酸酸化,再滴加KSCN溶液 | 溶液变成血红色 | Fe(N03)2试样已变质 |
B | 向甲苯中滴加少量酸性髙锰酸钾溶液. | 高锰酸钾溶液褪色 | 甲苯发生了氧化反应 |
C | 常温下分别测定浓度均为0.1mol/L的Na2SiO3溶液和Na2CO3溶液的pH | pH : Na2SiO3 >Na2C03 | 非金属性:Si>C |
D | 将少量某无色气体通入澄清石灰水中 | 出现白色沉淀 | 该气体一定是CO2 |
A. A B. B C. C D. D