题目内容
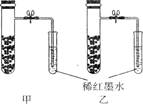
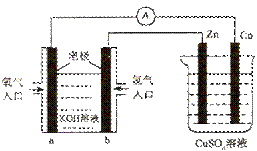
生活中常常有这样的现象:一件普通的铁器,如不精心保管,便会生锈;若不引起注意,锈斑蔓延开来,就会吞噬整个铁器使之变成废物。人们称这种现象为“锈吃铁”。请用相关学科知识解释“锈吃铁”这一自然现象。
首先是原电池的构成,铁器中铁作负极,其中杂质碳作正极,铁器表面的水膜构成电解液。?
(1)析氢腐蚀(负极):Fe-2e- Fe2+,正极反应:2H++2e-
Fe2+,正极反应:2H++2e- H2↑。析氢腐蚀后pH升高,从而发生吸氧腐蚀。?
H2↑。析氢腐蚀后pH升高,从而发生吸氧腐蚀。?
(2)吸氧腐蚀: Fe-2e- Fe2+,由于溶液中OH-浓度增大,生成Fe(OH)2,它很易被空气中的氧气所氧化:4Fe(OH)2+O2+2H2O
Fe2+,由于溶液中OH-浓度增大,生成Fe(OH)2,它很易被空气中的氧气所氧化:4Fe(OH)2+O2+2H2O 4Fe(OH)3,Fe(OH)3部分失水后生成海绵状物质Fe2O3·xH2O,它具有保湿作用,水膜的存在加速了铁器的腐蚀。
4Fe(OH)3,Fe(OH)3部分失水后生成海绵状物质Fe2O3·xH2O,它具有保湿作用,水膜的存在加速了铁器的腐蚀。
(1)析氢腐蚀(负极):Fe-2e-
 Fe2+,正极反应:2H++2e-
Fe2+,正极反应:2H++2e- H2↑。析氢腐蚀后pH升高,从而发生吸氧腐蚀。?
H2↑。析氢腐蚀后pH升高,从而发生吸氧腐蚀。?(2)吸氧腐蚀: Fe-2e-
 Fe2+,由于溶液中OH-浓度增大,生成Fe(OH)2,它很易被空气中的氧气所氧化:4Fe(OH)2+O2+2H2O
Fe2+,由于溶液中OH-浓度增大,生成Fe(OH)2,它很易被空气中的氧气所氧化:4Fe(OH)2+O2+2H2O 4Fe(OH)3,Fe(OH)3部分失水后生成海绵状物质Fe2O3·xH2O,它具有保湿作用,水膜的存在加速了铁器的腐蚀。
4Fe(OH)3,Fe(OH)3部分失水后生成海绵状物质Fe2O3·xH2O,它具有保湿作用,水膜的存在加速了铁器的腐蚀。铁在干燥的空气中不易生锈,但在潮湿的空气中发生了电化学腐蚀,腐蚀后生成的铁锈是一种海绵状的物质,具有保湿的作用,电解质水的存在促使铁器电化学腐蚀持续进行,直到铁器全部锈腐。?

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目