题目内容
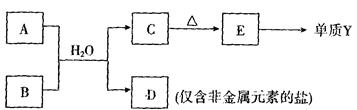
(7分)已知有以下物质相互转化。试回答:
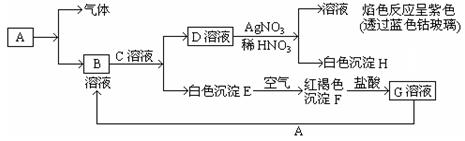
(1)写出B的化学式 ,D的化学式 。
(2)写出由D转变成H的离子方程式 。
(3)写出用KSCN鉴别G溶液的现象为 ;向G溶液加 入A的有关离子反应方程式 。
入A的有关离子反应方程式 。

(1)写出B的化学式 ,D的化学式 。
(2)写出由D转变成H的离子方程式 。
(3)写出用KSCN鉴别G溶液的现象为 ;向G溶液加
 入A的有关离子反应方程式 。
入A的有关离子反应方程式 。
略

练习册系列答案
相关题目
 得到H溶液,该无氧酸的阴离子在同主族元素形成的简单阴离子中还原性最强(除放射性元素)。其物质间转化关系如下图:(部分反应物和生成物略去)
得到H溶液,该无氧酸的阴离子在同主族元素形成的简单阴离子中还原性最强(除放射性元素)。其物质间转化关系如下图:(部分反应物和生成物略去)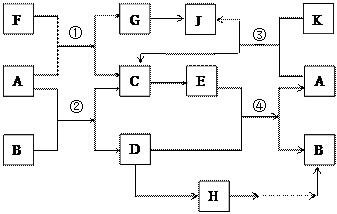

 (1)W的第一电离能比氧原子的 (填“大”或“小”),W的气态氢化物稳定性比
(1)W的第一电离能比氧原子的 (填“大”或“小”),W的气态氢化物稳定性比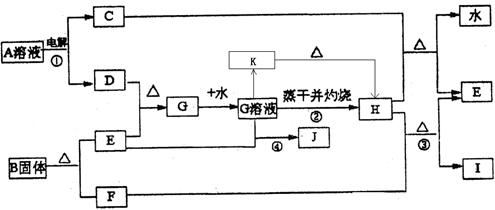
 则样品中G的质量分数为: 。
则样品中G的质量分数为: 。 种元素最高价氧化物的水化物的酸性最强的是 (填化学式),其中化学性质明显不同于其他三种化合物的
种元素最高价氧化物的水化物的酸性最强的是 (填化学式),其中化学性质明显不同于其他三种化合物的