��Ŀ����
����Ŀ������BaCl2��KCl�Ļ����ҺV L�������ֳ����ȷݡ�һ�ݵμ�ϡ���ᣬʹBa2+��ȫ����������a mol H2SO4����һ�ݵμ�AgNO3��Һ������b mol AgNO3ʹCl����ȫ������ԭ�����Һ�е�K+�����ʵ���Ũ��Ϊ______mol/L��
������������S ��SO32�� �� Fe2+ ��Al3+ ��Na ��HCl ��Na2O2�ڻ�ѧ��Ӧ��ֻ�ܱ���������______![]() �����
�����![]() ��ֻ�ܱ��ֳ������Ե���______
��ֻ�ܱ��ֳ������Ե���______![]() �����
�����![]() ��
��
��һ��������, PbO2��Cr3+��Ӧ��������Cr2O72����Pb2+������1 mol Cr3+��Ӧ����PbO2�����ʵ���Ϊ______mol��
����һ�������£�ʵ���ҷֱ��Թ������⡢������ء�����ء���������Ϊԭ����ȡ����,���Ƶ�ͬ��ͬѹ����ͬ���������ʱ���ĸ���Ӧ��ת�Ƶĵ�����֮��Ϊ______��
������ˮ�е�NO3�������ཡ������Σ����Ϊ�˽�������ˮ��NO3����Ũ�ȣ�ij�о���Ա����ڼ�����������Al�ۻ�ԭNO3����������N2�����ķ�Ӧ�ɱ�ʾ���£�����ɷ���ʽ����ƽ��____Al + ____NO3��+ ________ == ____AlO2�� + ____N2�� +____ H2O��
��ij��ѧ��Ӧ�ķ�Ӧ��Ͳ��![]()
�ٸ÷�Ӧ������������______��
�����÷�Ӧ����ʽ��I2��KIO3�ļ������ֱ���6��3�������±ߵĻ�ѧʽ���õ����ű������ת�Ƶķ������Ŀ��KMnO4 + KI + H2SO4��______��
���𰸡�![]() �� �� 1.5 1��2��2��1 10 6 4OH�� 10 3 2 I2��KIO3
�� �� 1.5 1��2��2��1 10 6 4OH�� 10 3 2 I2��KIO3 ![]()
��������
��BaCl2��NaCl�Ļ����ҺV L���������ֳ����ݣ�һ�ݵμ�ϡ���ᣬʹBa2+��ȫ����������a mol ���ᣬ��SO42�� + Ba2+ == BaSO4��
n(BaCl2) = a mol
��һ�ݵμ�AgNO3��Һ��ʹCl����ȫ��������Ӧ������b mol AgNO3,��
Ag+ + Cl�� == AgCl��
n(Cl��) = b mol
n(KCl) = b mol �C a mol��2 = (b �C 2a) mol

�ʴ�Ϊ��![]() ��
��
�Ƣ�������0�ۣ������м��̬���������������л�ԭ�ԣ�
����������������м��̬���������������л�ԭ�ԣ�
���������Ӵ����м��̬���������������л�ԭ�ԣ�
�������Ӵ�����ۣ�ֻ���������ԣ�
���Ƶ��ʴ�����ͼۣ�ֻ���л�ԭ�ԣ�
��HCl�������ۣ��ȴ�����ͼۣ���˾������������л�ԭ�ԣ�
�߹������ƴ����м��̬����˾������������л�ԭ�ԣ�
�ڻ�ѧ��Ӧ��ֻ�ܱ��������Ǣݣ�ֻ�ܱ��ֳ������Ե��Ǣܣ�
�ʴ�Ϊ�ݣ��ܣ�
����һ�������£�PbO2����Һ��Cr3+��Ӧ��������Cr2O72����Pb2+����Ӧ��Cr�ļ�̬������3�ۣ�pb�Ļ��ϼ۽���2�ۣ����ݵ����غ㣬������1 mol Cr3+��Ӧ����PbO2�����ʵ���Ϊ1.5 mol��
�ʴ�Ϊ��1.5��
���ø�����ء����������������Ӧ������O��-2��ת��Ϊ0�ۣ�������1 mol��������ת��4mol���ӣ����ù����������������������O����-1��ת��Ϊ0�ۣ�������1 mol��������ת��2 mol���ӣ����Ƶ�ͬ��ͬѹ����ͬ���������ʱ���ĸ���Ӧ��ת�Ƶĵ�����֮��Ϊ1��2��2��1��
�ʴ�Ϊ��1��2��2��1��
�ɷ�Ӧ��Al��AlO2����AlԪ�ػ��ϼ���0������Ϊ+3�ۣ�������3�ۣ�NO3����N2����Ԫ�ػ��ϼ���+5�۽���Ϊ0�ۣ�������10�ۣ����ϼ�������С������Ϊ30����Al��ϵ��Ϊ10��N2ϵ��Ϊ3���ɵ�Ԫ���غ��֪ϵ��Ϊ6����AlԪ���غ��֪ϵ��Ϊ10���ɵ���غ��֪ϵ��Ϊ����HԪ���غ��֪ϵ��Ϊ������ƽ�����ӷ���ʽΪ��
10Al + 6 NO3��+ 4OH�� == AlO2�� + 3 N2�� + 2 H2O��
�ʴ�Ϊ��10��6��4OH����10��3��2��
�ʢٷ�Ӧ��MnԪ�ػ��ϼ۽��ͣ�����ԭ��IԪ�ػ��ϼ���-1�۷ֱ�仯Ϊ0�ۡ�+5�ۣ���I2��KIO3Ϊ�������
�ʴ�Ϊ��I2��KIO3��
�����÷�Ӧ����ʽ��I2��KIO3�ļ������ֱ���6��3����IԪ��ʧȥ���ӵ���ĿΪ
2��6(1-0)+3��[5-(-1)]=30������ת�Ʒ������Ŀ�ɱ�ʾΪ![]() ,
,
�ʴ�Ϊ��![]() ��
��

����Ŀ���о���������ʴ�����з�������ȷ����
��� | �� | �� | �� |
ʵ�� |
|
|
|
���� | 8Сʱδ�۲� ��������ʴ | 8Сʱδ�۲� ��������ʴ | 1Сʱ�۲� ��������ʴ |
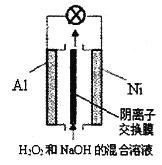
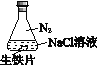
A. ���У�NaCl��Һ���ܽ��O2������ʹ����Ƭ������ʴ
B. ���У�����Ƭδ������ʴ��ԭ��֮һ��ȱ��H2O
C. ����������Ӧ��O2+4e+ 2H2O ==4OH
D. �ԱȢ٢ڢۣ�˵�����ܸ���O2