题目内容
含有硒(Se)的保键品已进入市场,已知该元素与氧具有相同的最外层电子数。则下列关于硒的叙述中不正确的是 ( )


A.最高价氧化物的化学式为SeO3 | B.单质Se是一种半导体材料 | C.原子半径比硫大,比溴小 | D.单质的氧化性比氯气弱,比溴强,比O3弱 |
CD
 本题解题的关键在于搞清楚Se与O、S、Cl、Br等元素在元素周期表中的相对位置关系及Se单质和臭氧的特殊性质。如Se可作为半导体材料,臭氧是很强的氧化剂等。另外元素周期律的知识是判断选项正误的钥匙。
本题解题的关键在于搞清楚Se与O、S、Cl、Br等元素在元素周期表中的相对位置关系及Se单质和臭氧的特殊性质。如Se可作为半导体材料,臭氧是很强的氧化剂等。另外元素周期律的知识是判断选项正误的钥匙。 Se位于元素周期表的第ⅥA族,最外层为6个电子,故最高价为+6价,最低价为-2价,因此最高价氧化物的形式为SeO3。再由于Se原子半径较S原子的大,故体现部分金属性质。硒可作为半导体材料。因此选项A、B都正确。
Se位于元素周期表的第ⅥA族,最外层为6个电子,故最高价为+6价,最低价为-2价,因此最高价氧化物的形式为SeO3。再由于Se原子半径较S原子的大,故体现部分金属性质。硒可作为半导体材料。因此选项A、B都正确。 根据O、S、Cl、Br与Se在元素周期表中的相对位置关系,运用元素周期律的知识不难判断出原子半径大小关系为:Se>S、Se>Br;单质的氧化性的关系为O3>O2>S>Se、Cl2>Br2>Se,因此可判断C、D两选项中的部分判断存在错误。
根据O、S、Cl、Br与Se在元素周期表中的相对位置关系,运用元素周期律的知识不难判断出原子半径大小关系为:Se>S、Se>Br;单质的氧化性的关系为O3>O2>S>Se、Cl2>Br2>Se,因此可判断C、D两选项中的部分判断存在错误。
练习册系列答案
相关题目
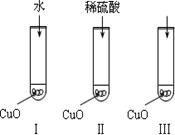
 (1)某同学提出的假设是 ;
(1)某同学提出的假设是 ;

 SO3+NO ②SO3+H2O
SO3+NO ②SO3+H2O