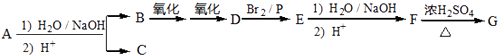��Ŀ����
����Ŀ��ij��ѧ��ȤС�鰴���������̽��С���þ���Ͻ��Ʊ����������塱��ʵ����ͼ1��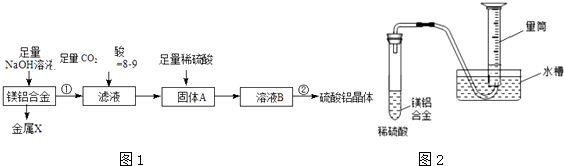
��1��д����������ˮ�еĵ��뷽��ʽ ��
��2��þ���Ͻ��м�NaOH��Һ�����ӷ�Ӧ����ʽΪ �� ��Һ��ͨ������CO2�Ļ�ѧ����ʽ
��3�������ڰ����IJ���������Ũ���������ˡ����
��4������X��CO2��ȼ�յĻ�ѧ����ʽ
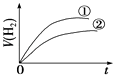
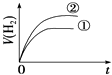
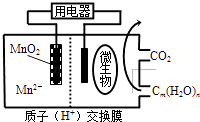
��5������ȤС��Ϊ�ⶨþ���Ͻ��и���ɵ����������������ͼ2װ�ã�����Ҫ�ⶨ�����ݣ��¶ȡ�ѹǿ���⣩���� ��
���𰸡�
��1��Al2��SO4��3=2Al3++3SO ![]()
��2��2Al+2OH��+2H2O=2AlO ![]() +3H2����NaAlO2+CO2+2H2O=Al��OH��3+NaHCO3
+3H2����NaAlO2+CO2+2H2O=Al��OH��3+NaHCO3
��3����ȴ�ᾧ�����½ᾧ��
��4��2Mg+CO2 ![]() 2MgO+C
2MgO+C
��5�������������þ���Ͻ������
���������⣺þ���ܼӦ����NaOH��Һ�Ƚ�þ�����벢�õ�ƫ��������Һ������Һ�����ữ�õ������������������Ǻ��ܽ���ϡ�����У������������Һ���������ᾧ���ȵ�Ŀ������1��������Ϊǿ����ʣ���ˮ�еĵ��뷽��ʽΪAl2��SO4��3=2Al3++3SO ![]() �����Դ��ǣ�Al2��SO4��3=2Al3++3SO
�����Դ��ǣ�Al2��SO4��3=2Al3++3SO ![]() ����2����þ���Ͻ��м�����������������Һ��Al������������Һ���ɿ����Ե�ƫ�����ƣ�þ����Ӧ��������Ӧ�����ӷ���ʽΪ2Al+2OH��+2H2O=2AlO
����2����þ���Ͻ��м�����������������Һ��Al������������Һ���ɿ����Ե�ƫ�����ƣ�þ����Ӧ��������Ӧ�����ӷ���ʽΪ2Al+2OH��+2H2O=2AlO ![]() +3H2������Һ�к���NaAlO2 �� ͨ������CO2�Ļ�ѧ����ʽΪNaAlO2+CO2+2H2O=Al��OH��3+NaHCO3 �� ���Դ��ǣ�2Al+2OH��+2H2O=2AlO2��+3H2����NaAlO2+CO2+2H2O=Al��OH��3+NaHCO3����3������������IJ���������Ũ������ȴ�ᾧ�����½ᾧ��������ϴ�ӡ�������Դ��ǣ���ȴ�ᾧ�����½ᾧ������4��þ�Ͷ�����̼�ڵ�ȼ�����·�Ӧ��������þ��̼����Ӧ�Ļ�ѧ����ʽΪ2Mg+CO2
+3H2������Һ�к���NaAlO2 �� ͨ������CO2�Ļ�ѧ����ʽΪNaAlO2+CO2+2H2O=Al��OH��3+NaHCO3 �� ���Դ��ǣ�2Al+2OH��+2H2O=2AlO2��+3H2����NaAlO2+CO2+2H2O=Al��OH��3+NaHCO3����3������������IJ���������Ũ������ȴ�ᾧ�����½ᾧ��������ϴ�ӡ�������Դ��ǣ���ȴ�ᾧ�����½ᾧ������4��þ�Ͷ�����̼�ڵ�ȼ�����·�Ӧ��������þ��̼����Ӧ�Ļ�ѧ����ʽΪ2Mg+CO2 ![]() 2 MgO+C�����Դ��ǣ�2Mg+CO2
2 MgO+C�����Դ��ǣ�2Mg+CO2 ![]() 2 MgO+C����5��ij��ȤС��Ϊ�ⶨþ���Ͻ��и���ɵ���������������ͼ��֪���ܹ����������������ݽ���������֮��Ĺ�ϵʽ����֪�����ͼ1ʾװ����Ҫ�ⶨ�������������������þ���Ͻ�����������Դ��ǣ������������þ���Ͻ��������
2 MgO+C����5��ij��ȤС��Ϊ�ⶨþ���Ͻ��и���ɵ���������������ͼ��֪���ܹ����������������ݽ���������֮��Ĺ�ϵʽ����֪�����ͼ1ʾװ����Ҫ�ⶨ�������������������þ���Ͻ�����������Դ��ǣ������������þ���Ͻ��������

 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д�����Ŀ���ݡ��ο���Ϣ���������п�ѧ��������ǡ�21���͵���Դ������δ����ʯ�͡��Ĺ۵㣮
��1���������������ȼ�յ��Ȼ�ѧ����ʽΪSi��s��+O2��g���TSiO2��s����H=��989.2kJmol��1 �� �йؼ����������±���
��ѧ�� | Si��O | O=O | Si��Si |
����kJmol��1 | x | 498.8 | 176 |
��֪1molSi�к�2molSi��Si����1molSiO2�к�4molSi��O������x��ֵΪ ��
��2���������Ϊһ���ձ�ʹ�õ�������Դ���������ã��������������ص�����˵���У�����Ϊ�������� ��
A.��������䡢���棬�Ӱ�ȫ�Ƕȿ��ǣ�������ѵ�ȼ��
B.�����Դ�ḻ�����ڿ��ɣ��ҿ�����
C.��ȼ�շų�����������ȼ�ղ���Ի�����Ⱦ�̶ȵͣ�������Ч����
D.Ѱ�Ҹ�Ч�´���������ʹ��ӦSiO2+2C ![]() Si+2CO���ڳ����·������ǹ���Դ�������õĹؼ�����
Si+2CO���ڳ����·������ǹ���Դ�������õĹؼ�����
��3����ҵ�Ʊ�����ķ�ӦΪ2H2��g��+SiCl4��g���TSi��s��+4HCl��g����H=+240.4kJmol��1 �� ���ɵ�HClͨ��100mL 1molL��1��NaOH��Һǡ����ȫ�����գ��������Ʊ�����ķ�Ӧ������������ա����ͷš���������ΪkJ��