题目内容
现有H2SO4和Na2SO4混合溶液200 mL,其中硫酸的物质的量浓度为1 mol·L-1,硫酸钠的物质的量浓度为0.5 mol·L-1。若要使硫酸和硫酸钠的物质的量浓度分别为2 mol·L-1和0.2 mol·L-1,应加入质量分数为55.8%的硫酸溶液(ρ="1.35" g·mL-1)多少毫升后再加蒸馏水配制?
应加入质量分数为55.8%的硫酸溶液(ρ="1.35" g·mL-1)58.1 mL后再加蒸馏水配制。?
设加入V mL质量分数为55.8%的硫酸溶液,加水后溶液的体积为V (总)。
根据H2SO4的物质的量得:200 mL×10-3 L·mL-1×1 mol·L-1+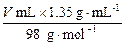 =
=
V (总)·2 mol·L-1。
根据Na2SO4的物质的量得:200 mL×10-3 L·mL-1×0.5 mol·L-1=V (总)·2 mol·L-1
计算得:V="58.1" mL,V (总)="0.5" L。
根据H2SO4的物质的量得:200 mL×10-3 L·mL-1×1 mol·L-1+
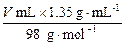 =
=V (总)·2 mol·L-1。
根据Na2SO4的物质的量得:200 mL×10-3 L·mL-1×0.5 mol·L-1=V (总)·2 mol·L-1
计算得:V="58.1" mL,V (总)="0.5" L。

练习册系列答案
 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目

 ②m g该氯原子的物质的量为
②m g该氯原子的物质的量为 mol ③该氯原子的摩尔质量是aNa g ④n g该氯原子所含的电子数是
mol ③该氯原子的摩尔质量是aNa g ④n g该氯原子所含的电子数是