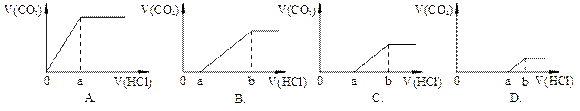题目内容
(10分)含有SiO2的石灰石5 g和0.267 L 0.5 mol·L-1的盐酸反应,所得CO2在标准状况下的体积为1 064 mL。
(1)要中和剩余的盐酸,需1 mol·L-1的NaOH溶液的体积多少毫升?
(2)煅烧这种不纯的石灰石1 t,最后残留固体的质量是多少?
(1)要中和剩余的盐酸,需1 mol·L-1的NaOH溶液的体积多少毫升?
(2)煅烧这种不纯的石灰石1 t,最后残留固体的质量是多少?
(1)38.5 mL (2)0.582 t
CO2的物质的量为1.064 L/22.4 L·mol-1="0.047" 5 mol,则5 g石灰石含碳酸钙:0.047 5 mol×100 g·mol-1="4.75" g,消耗盐酸:0.047 5 mol×2="0.095" mol,剩余盐酸:0.267 L×0.5 mol·L-1-0.095 mol="0.133" 5 mol-0.095 mol="0.038" 5 mol,要中和剩余的盐酸,需1 mol·L-1的NaOH溶液的体积为0.038 5 mol/1 mol·L-1="0.038" 5 L="38.5" mL;煅烧这种不纯的石灰石1 t,最后残留固体的质量为1 t×[(5-4.75)/5]+1 t×(4.75/5)×(56/100)="0.582" t。

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
 CO2
CO2 2CO
2CO Na2SiO3+CO2↑可知硅酸的酸性比碳酸的酸性强
Na2SiO3+CO2↑可知硅酸的酸性比碳酸的酸性强