题目内容
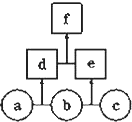
【题目】NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体.相应的实验过程如图:
(1)写出上述实验过程中所用试剂(写化学式):试剂①;试剂③ .
(2)判断试剂①已过量的方法是: .
(3)用化学方程式表示加入试剂②的作用:
(4)操作①是利用半透膜进行分离提纯.操作①的实验结果:淀粉(填“能”或“不能”)透过半透膜;SO ![]() (填“能”或“不能”)透过半透膜;请用实验证明上述结果,完成下表(可不填满,也可增加):限选试剂:1mol/L AgNO3溶液、1mol/L BaCl2溶液、1mol/L Ba(NO3)2溶液、碘水、稀盐酸、稀硝酸
(填“能”或“不能”)透过半透膜;请用实验证明上述结果,完成下表(可不填满,也可增加):限选试剂:1mol/L AgNO3溶液、1mol/L BaCl2溶液、1mol/L Ba(NO3)2溶液、碘水、稀盐酸、稀硝酸
编号 | 实验操作 | 预期现象和结论 |
① |
|
|
② |
|
|
【答案】
(1)BaCl2;HCl
(2)静置,向上层清液中滴加少量氯化钡溶液,没有白色沉淀产生,说明氯化钡溶液已过量
(3)BaCl2+Na2CO3=2NaCl+BaCO3↓、CaCl2+Na2CO3=2NaCl+CaCO3↓
(4)不能;能;取半透膜外液体,加入少量碘水;液体没有变成蓝色,证明淀粉不能透过半透膜;另取半透膜外液体,加入足量稀盐酸和少量1mol/L BaCl2溶液;产生不溶于盐酸的白色沉淀,证明SO42﹣能够透过半透膜
【解析】解:胶体不能透过半透膜,操作①为渗析,除去Na2SO4、CaCl2 , 可分别加入BaCl2、Na2CO3 , 除去粗盐中含有的Ca2+、SO42﹣可溶性杂质的方法:加入过量BaCl2 , 去除硫酸根离子;再加入过量Na2CO3(去除钙离子),则试剂①为BaCl2 , 操作②为过滤,沉淀A为硫酸钡,试剂②为Na2CO3 , 操作③为过滤,沉淀B为碳酸钙和碳酸钡,试剂③为盐酸,加入盐酸可除去过量的Na2CO3 , 最后蒸发结晶可得到NaCl晶体,(1)由以上分析可知试剂①为BaCl2 , 试剂③为HCl,所以答案是:BaCl2;HCl;(2)判断试剂①已过量的方法是静置,向上层清液中滴加少量氯化钡溶液,没有白色沉淀产生,说明氯化钡溶液已过量,所以答案是:静置,向上层清液中滴加少量氯化钡溶液,没有白色沉淀产生,说明氯化钡溶液已过量;(3)试剂②为Na2CO3 , 加入试剂②的作用是除去溶液中钙离子和过量的钡离子,反应的化学方程式为BaCl2+Na2CO3=2NaCl+BaCO3↓、CaCl2+Na2CO3=2NaCl+CaCO3↓,所以答案是:BaCl2+Na2CO3=2NaCl+BaCO3↓、CaCl2+Na2CO3=2NaCl+CaCO3↓;(4)胶体粒子和浊液粒子半径比较大,不能透过半透膜,而溶质粒子可通过半透膜,检验淀粉,可取半透膜外液体,加入少量碘水,液体没有变成蓝色,证明淀粉不能透过半透膜,检验SO42﹣ , 可另取半透膜外液体,加入足量稀盐酸和少量1mol/L BaCl2溶液,产生不溶于盐酸的白色沉淀,证明SO42﹣能够透过半透膜.所以答案是:不能; 能;
编号 | 实验操作 | 预期现象和结论 |
① | 取半透膜外液体,加入少量碘水 | 液体没有变成蓝色,证明淀粉不能透过半透膜 |
② | 另取半透膜外液体,加入足量稀盐酸和少量1mol/L BaCl2溶液 | 产生不溶于盐酸的白色沉淀,证明SO42﹣能够透过半透膜 |

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案【题目】某pH=1的ZnCl2和HCl的混合溶液中含有FeCl3杂质,为了除去FeCl3杂质,需将溶液调至pH=4.在调节溶液pH值时,应选用的试剂是( )
A.NaOH
B.ZnO
C.Zn
D.Fe2O3
【题目】卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
(1)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的.使氢氟酸分子缔合的作用力是 .
(2)请根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是 .
氟 | 氯 | 溴 | 碘 | |
第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
(3)已知高碘酸有两种形式,化学式分别为H5IO6(结构如上图)和HIO4 , 前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6HIO4 . (填“>”、“<”或“=”)
(4)碘在水中的溶解度虽然小,但在碘化钾溶液中溶解度却明显增大这是由于溶液中发生下列反应I﹣+I2=I3﹣ . I3﹣离子的中心原子周围σ键电子对对数为 . 与KI3类似的,还有CsICl2等.已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列式发生.
A.CsICl2=CsCl+ICl B.CsICl2=CsI+Cl2
(5)已知CaF2晶体的密度为ρg/cm3 , NA为阿伏加德罗常数,CaF2晶胞的边长为a pm,则CaF2的相对分子质量可以表示为(用含a的式子表示).