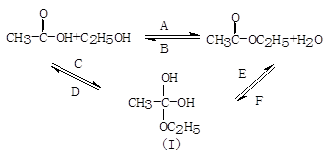题目内容
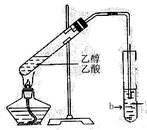
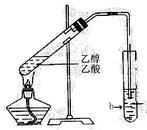
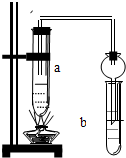 如图所示,在试管a中先加2mL乙醇,边摇动边缓缓加入5mL浓硫酸,摇匀冷却后,再加入2g无水醋酸钠,充分搅动后,固定在铁架台上.在试管b中加入适量的饱和Na2CO3溶液.连接好装置,给a加热,当观察到试管b中有明显现象时,停止实验.
如图所示,在试管a中先加2mL乙醇,边摇动边缓缓加入5mL浓硫酸,摇匀冷却后,再加入2g无水醋酸钠,充分搅动后,固定在铁架台上.在试管b中加入适量的饱和Na2CO3溶液.连接好装置,给a加热,当观察到试管b中有明显现象时,停止实验.①如图所示的装置中,哪些地方有明显错误的?
②写出试管a中的主要反应方程式
CH3COOH+C2H5OH
CH3COOC2H5+H2O
| 浓硫酸 |
| △ |
CH3COOH+C2H5OH
CH3COOC2H5+H2O
| 浓硫酸 |
| △ |
③饱和Na2CO3溶液的作用是
除去乙酸和乙醇(降低乙酸乙酯的溶解度)
除去乙酸和乙醇(降低乙酸乙酯的溶解度)
④右边的球形管除冷凝作用外,另一个作用是
防止倒吸
防止倒吸
.分析:①给浓硫酸、乙酸、乙醇的混合液体加热,试管应该倾斜;a装置内导管伸入的过长;
②酯化反应的本质为酸脱羟基,醇脱氢,该反应生成乙酸乙酯和水,且为可逆反应;
③实验室里用饱和碳酸钠溶液冷却乙酸乙酯的原因:一是利用碳酸钠溶液中的水溶解乙醇(乙醇在水里的溶解度大于乙酸乙酯),二是碳酸钠能跟乙酸反应吸收乙酸,便于闻到乙酸乙酯的香味,而乙酸乙酯难溶于饱和碳酸钠溶液,这样就可以获得较为纯净的乙酸乙酯液体;
④乙酸乙酯中混有乙醇和乙酸,二者易溶于水而产生倒吸,球形漏斗由于容积较大,能起到防止倒吸的作用.
②酯化反应的本质为酸脱羟基,醇脱氢,该反应生成乙酸乙酯和水,且为可逆反应;
③实验室里用饱和碳酸钠溶液冷却乙酸乙酯的原因:一是利用碳酸钠溶液中的水溶解乙醇(乙醇在水里的溶解度大于乙酸乙酯),二是碳酸钠能跟乙酸反应吸收乙酸,便于闻到乙酸乙酯的香味,而乙酸乙酯难溶于饱和碳酸钠溶液,这样就可以获得较为纯净的乙酸乙酯液体;
④乙酸乙酯中混有乙醇和乙酸,二者易溶于水而产生倒吸,球形漏斗由于容积较大,能起到防止倒吸的作用.
解答:解:①盛有混合液体的a试管不能直立放置,伸入a试管的导管太长,
答:图中装置错误有:a试管垂直放置;伸入a试管的导管过长;
②酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应方程式为:CH3COOH+C2H5OH
CH3COOC2H5+H2O,
故答案为:CH3COOH+C2H5OH
CH3COOC2H5+H2O;
③碳酸钠溶液中的水溶解乙醇,能跟乙酸反应吸收乙酸,便于闻到乙酸乙酯的香味,降低乙酸乙酯的溶解度,使乙酸乙酯难溶于饱和碳酸钠溶液,便于分层,
故答案为:除去乙酸和乙醇(降低乙酸乙酯的溶解度);
④乙酸乙酯中混有乙醇和乙酸,二者易溶于水而产生倒吸,球形漏斗由于容积较大,能起到防止倒吸的作用,故答案为:防倒吸.
答:图中装置错误有:a试管垂直放置;伸入a试管的导管过长;
②酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应方程式为:CH3COOH+C2H5OH
| 浓硫酸 |
| △ |
故答案为:CH3COOH+C2H5OH
| 浓硫酸 |
| △ |
③碳酸钠溶液中的水溶解乙醇,能跟乙酸反应吸收乙酸,便于闻到乙酸乙酯的香味,降低乙酸乙酯的溶解度,使乙酸乙酯难溶于饱和碳酸钠溶液,便于分层,
故答案为:除去乙酸和乙醇(降低乙酸乙酯的溶解度);
④乙酸乙酯中混有乙醇和乙酸,二者易溶于水而产生倒吸,球形漏斗由于容积较大,能起到防止倒吸的作用,故答案为:防倒吸.
点评:本题考查乙酸乙酯的制备,题目难度不大,本题注意把握乙酸乙酯的制备原理和实验方法,学习中注重实验评价能力的培养.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
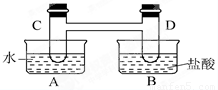
 I、如图所示,在容器A中装有20℃的水50mL,容器B中装有1mol/L的盐酸50mL,试管C、D相连通,且其中装有红棕色NO2和无色N2O4的混合气体,并处于下列平衡:2NO2?N2O4△H=-57kJ/mol,当向A中加入50gNH4NO3晶体使之溶解;向B中加入2g苛性钠时:
I、如图所示,在容器A中装有20℃的水50mL,容器B中装有1mol/L的盐酸50mL,试管C、D相连通,且其中装有红棕色NO2和无色N2O4的混合气体,并处于下列平衡:2NO2?N2O4△H=-57kJ/mol,当向A中加入50gNH4NO3晶体使之溶解;向B中加入2g苛性钠时: