题目内容
NO2、NO是大气的污染物,可用NaOH溶液吸收,发生的有关化学反应方程式为:N2O4?2NO2,2NO2+2NaOH=NaNO2+NaNO3+H2O,NO2+NO+2NaOH=2NaNO2+H2O.现有a升NO2(其中还含有20%的N2O4)和b升NO的混合气体,被200mlNaOH溶液完全吸收,则
的值可能是(气体体积均已折算为标准状况下)( )
| a |
| b |
分析:由方程式2NO2+2NaOH=NaNO2+NaNO3+H2O,NO2+NO+2NaOH=2NaNO2+H2O可知,NO单独不能被吸收,NO和NO2混合气体被NaOH溶液被完全吸收,满足n(NO2):n(NO)≥1,把N2O4折换成NO2,计算a、b的关系即可解答.
解答:解:由方程式2NO2+2NaOH=NaNO2+NaNO3+H2O,NO2+NO+2NaOH=2NaNO2+H2O可知,NO单独不能被吸收,NO和NO2混合气体被NaOH溶液被完全吸收,满足n(NO2):n(NO)≥1,aLNO2,其中N2O4的体积分数是20%,N2O4?2NO2,把N2O4折换成NO2,NO2的体积总共为aL×(1-20%)+aL×20%×2=1.2aL,
≥1,所以
≥
≈0.83,
故选BD.
| 1.2a |
| b |
| a |
| b |
| 5 |
| 6 |
故选BD.
点评:本题考查了NO2、NO是大气的污染物的处理,理顺二氧化氮、一氧化氮混合气体和氢氧化钠间反应的关系是解答的关键,题目难度中等.

练习册系列答案
相关题目
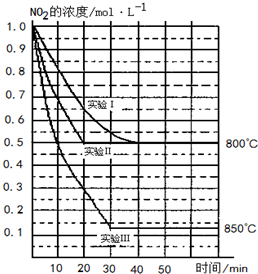 某条件下,在2L密闭容器中发生如下反应2NO2(g)?2NO(g)+O2(g)
某条件下,在2L密闭容器中发生如下反应2NO2(g)?2NO(g)+O2(g) 2NO(g)+O2(g)
2NO(g)+O2(g) 2NO(g)+O2(g)体系中,n (NO2)随时间的变化如表:
2NO(g)+O2(g)体系中,n (NO2)随时间的变化如表: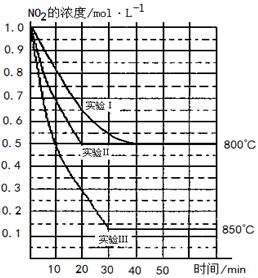
 2NO(g)+O2(g)
2NO(g)+O2(g) 2NO(g)+O2(g)体系中,n (NO2)随时间的变化如表:
2NO(g)+O2(g)体系中,n (NO2)随时间的变化如表: