题目内容
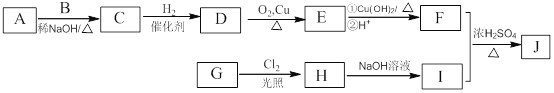
【题目】下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。

(1)单质F的化学式是_______________。
(2)写出单质B与强碱溶液反应的离子方程式___________________________,写出由沉淀J生成H溶液的离子方程式______________________________________。
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式:____________________________________________,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式______________________________。
(4)溶液I中所含金属离子是__________________。
【答案】 H2 2Al+2OH-+2H2O===2AlO![]() +3H2↑ Al(OH)3+OH-===AlO
+3H2↑ Al(OH)3+OH-===AlO![]() +2H2O Fe2++2NH3·H2O===Fe(OH)2↓+ 2NH4+ 4Fe(OH)2+O2+2H2O===4Fe(OH)3 Na+、Al3+
+2H2O Fe2++2NH3·H2O===Fe(OH)2↓+ 2NH4+ 4Fe(OH)2+O2+2H2O===4Fe(OH)3 Na+、Al3+
【解析】金属B与强碱反应得到单质F与H,则B为Al、F为H2,H为偏铝酸盐,G为红褐色沉淀,则G为Fe(OH)3,红棕色物质A与金属Al发生置换反应生成单质C与氧化物D,则A为Fe2O3、C为Fe、D为Al2O3,由转化关系可知,E为FeCl2,H为NaAlO2,溶液I为NaCl、HCl、AlCl3混合物,J为Al(OH)3,则
(1)由上述分析可知,单质F的化学式是H2;(2)单质Al与强碱溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO![]() +3H2↑,由沉淀J生成 H溶液的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O;(3)溶液FeCl2中加入氨水时,先生成白色沉淀L为氢氧化亚铁,离子方程式:Fe2++2NH3·H2O=Fe(OH)2↓+ 2NH4+,白色沉淀会迅速变为灰绿色,最终变为红褐色沉淀,L变为G的化学反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;(4)溶液I为NaCl、HCl、AlCl3混合物,所含金属离子是Na+、Al3+。
+3H2↑,由沉淀J生成 H溶液的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O;(3)溶液FeCl2中加入氨水时,先生成白色沉淀L为氢氧化亚铁,离子方程式:Fe2++2NH3·H2O=Fe(OH)2↓+ 2NH4+,白色沉淀会迅速变为灰绿色,最终变为红褐色沉淀,L变为G的化学反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;(4)溶液I为NaCl、HCl、AlCl3混合物,所含金属离子是Na+、Al3+。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】分子式为C3H6O2的有机物有多种同分异构体,现有其中的四种X、Y、Z、W,它们的分子中均含甲基,将它们分别进行下列实验以鉴别,其实验记录如下:
NaOH溶液 | 银氨溶液 | 新制Cu(OH)2 | 金属钠 | |
X | 中和反应 | 无现象 | 溶解 | 产生氢气 |
Y | 无现象 | 有银镜 | 加热后有砖红色沉淀 | 产生氢气 |
Z | 水解反应 | 有银镜 | 加热后有砖红色沉淀 | 无现象 |
W | 水解反应 | 无现象 | 无现象 | 无现象 |
回答下列问题:
(1)写出X的结构简式________, W的系统命名是________.
(2)①Y在一定条件下发生分子内的脱水反应的化学方程式_________________________
②Z与NaOH溶液反应的化学方程式_______________________________
【题目】A和B两种有机物可以互溶,有关性质如下
密度(20℃) | 熔点(℃) | 沸点(℃) | 溶解性 | |
A | 0.7893 | -117.3 | 78.5 | 与水以任意比混溶 |
B | 0.7137 | -116.6 | 34.5 | 不溶于水 |
(1)要除去A和B的混合物中的少量B,可采用________方法即可得到A。
A.蒸馏 B.重结晶 C.萃取 D.加水充分振荡,分液
(2)将有机物A置于氧气流中充分燃烧,A和氧气恰好完全反应消耗氧气6.72L(标准状况),生成5.4g H2O和8.8g CO2,则该物质的分子式是______;已知有机物A的核磁共振氢谱如下图所示,则A的结构简式为_______________。以A为原料可以合成M,M可做内燃机的抗冻剂,M与A所含碳原子数相等,M的官能团与A相同,但官能团数目是A的两倍,请写出以A为原料制取M的合成路线:_______________。

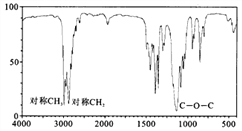
(3)若质谱图显示B的相对分子质量为74,红外光谱如图所示,则B的结构简式为____________。
(4)准确称取一定质量的A和B的混合物,在足量氧气中充分燃烧,将产物依次通过足量的无水氯化钙和碱石灰,发现质量分别增重14.4g和26.4g。计算混合物中A和B的物质的量之比___________。