题目内容
还原某二价金属的氧化物4克,需0.2mol电子,则该金属元素的相对原子质量为( )
| A.24 | B.40 | C.56 | D.64 |
设金属元素为R,金属氧化物的物质的量为X.
RO→R转移电子
1mol 2mol
X 0.2mol
X=0.1mol,
金属氧化物的摩尔质量=
=40g/mol,金属氧化物的相对分子质量为40,所以金属原子的相对原子质量为40-16=24,故选A.
RO→R转移电子
1mol 2mol
X 0.2mol
X=0.1mol,
金属氧化物的摩尔质量=
| 4g |
| 0.1mol |

练习册系列答案
相关题目

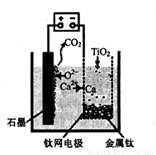

 Cr2O72-+H2O在酸性条件下+6价铬化合物具有强氧化性,可以将C2H5OH氧化为CH3COOH,本身被还原为Cr3+,Cr3+在水溶液中呈灰绿色。
Cr2O72-+H2O在酸性条件下+6价铬化合物具有强氧化性,可以将C2H5OH氧化为CH3COOH,本身被还原为Cr3+,Cr3+在水溶液中呈灰绿色。